Le nom du chrome provient du grec khrỗma signifiant couleur qui fait référence aux nombreux composés colorés du chrome. En 1761, Johann Gottlob Lehmann découvre un minéral rouge-orangé dans les montagnes de l’Oural qu’il nomme crocoïte. En 1797, Louis Nicolas Vauquelin utilise des échantillons de ce minéral pour en extraire de l’oxyde de chrome. Il isola l’élément pur en 1798.
La découverte de la première utilisation du chrome a été faite en analysant des flèches, sans aucun signe de corrosion, datant du IIIe siècle avant Jésus Christ trouvées dans le Mausolée de l’empereur Qin Shi Huang, fondateur de la dynastie Qin, en Chine.
Données physico-chimiques
Données atomiques
| Numéro atomique | Masse atomique | Configuration électronique | Structure cristalline | Rayon métallique pour la coordinence 12 |
| 24 | 52,00 g.mol-1 | [Ar] 3d5 4s1 | cubique centrée de paramètre a = 0,288 nm | 136,0 pm |
Données physiques
| Masse volumique | Dureté | Température de fusion | Température d’ébullition | Conductibilité électrique | Conductibilité thermique | Solubilité dans l’eau |
| 7,20 g.cm-3 | 7,5 | 1 857°C | 2 672°C | 7,74.106 S.m-1 | 93,7 W.m-1.K-1 | insoluble |
Données chimiques
| Électronégativité de Pauling |
pKa : HCrO4–/CrO42-aq |
pKa : Craq3+/CrOH2+aq |
pKa : HCr2O7–/Cr2O72- | pKs : Cr(OH)2 | pKs : Cr(OH)3 |
| 1,66 | 6,5 | 3,9 | 0 | 17,0 | 30 |
Potentiels standards :
| Cr3+ + e = Cr2+ | E°= -0,41 V |
| Cr2O72- + 14H+ + 6e = 2Cr3+ + 7H2O | E° = 1,33 V |
| HCrO4– + 7H+ + 3e = Cr3+ + 4H2O | E° = 1,20 V |
| CrO42- + 4H2O + 3e = Cr(OH)3(s) + 5OH– | E° = -0,13 V |
| Cr3+ + 3e = Cr(s) | E°= -0,74 V |
| Cr2+ + 2e = Cr(s) | E°= -0,86 V |
Données thermodynamiques
Chrome cristallisé
|
Chrome gazeux
|
Données industrielles
Matières premières
La teneur moyenne de l’écorce terrestre est de 400 ppm.
Minerai
La chromite, FeCr2O4, qui possède une structure spinelle (MgAl2O4) dans laquelle les ions Mg2+ sont partiellement substitués par des ions Fe2+ et les ions Al3+ partiellement substitués par des ions Fe3+ et Cr3+ pour donner une formule du type : (Mg2+,Fe2+)(Al3+,Fe3+,Cr3+)2O4.
- Les minerais riches, contenant de 48 à 55 % de Cr2O3, avec un rapport Cr/Fe > 3, sont destinés à la fabrication des ferrochromes. Ils sont extraits particulièrement au Kazakhstan, en Turquie, Russie et Albanie. Ces gisements, podiformes, se présentent sous forme de lentilles de minerai. Ils sont exploités d’abord à ciel ouvert puis souterrainement lors de l’avancement de l’extraction.
- Les minerais pauvres, contenant environ 30 % de Cr2O3, avec un rapport Cr/Fe d’environ 1,6, initialement utilisés comme matériaux réfractaires sont, depuis l’introduction du procédé AOD d’élaboration des aciers inoxydables, également employés pour élaborer des ferrochromes à basse teneur en Cr (50-55 % de Cr et 6-8 % de C) appelés charge-chrome. Ces gisements se présentent sous forme de couches successives et sont appelés stratiformes. Ils sont exploités particulièrement en Afrique du Sud, en Inde, au Zimbabwe, en Finlande et au Brésil.
Les minerais sont enrichis, en général, par gravimétrie à l’aide de spirales ou de tables à secousses.
Le gisement du Bushveld
En Afrique du Sud, le gisement géant stratiforme du Bushveld s’étend sur 66 000 km2. Il est formé de couches peu épaisses, de moins de 1,5 m de minerai sur une épaisseur totale de 5 000 m et constitue, avec 3,1 milliards de t de minerai, les réserves les plus importantes au monde. Le Complexe du Bushveld est constitué de 3 lobes (ouest, nord et est) d’où provient toute la production minière de chrome, vanadium et platinoïdes d’Afrique du Sud. Le lobe ouest, le plus important, est situé au nord-ouest de Pretoria. L’une des couches de chromite, dénommée UG2 a la particularité d’être riche en platinoïdes. En conséquence elle est exploitée pour produire ces derniers, la chromite constituant un co-produit récupéré lors d’opérations de flottation qui séparent les platinoïdes, associés à des sulfures, de la chromite constituant la gangue (voir le chapitre platinoïdes). En 2018, la coproduction de chromite dans la couche UG2 représente 30 % de la production sud-africaine.
Carte du complexe du Bushveld publiée sur le site du Lycée de Bois d’Olive à La Réunion que nous remercions.

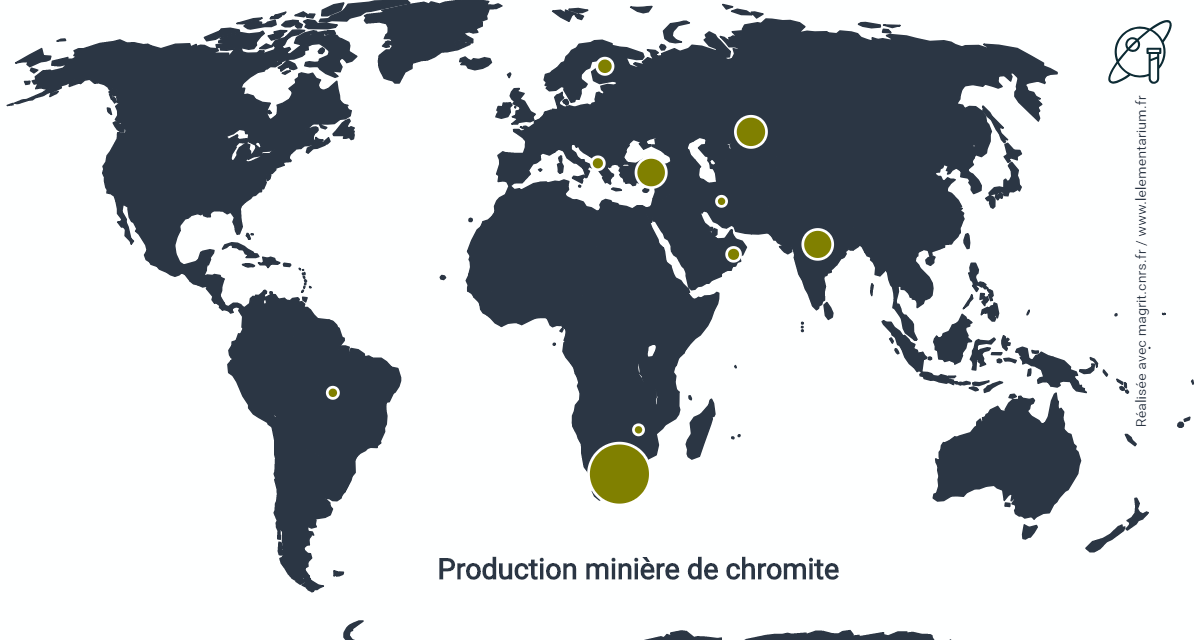
Production minière
En 2019, la production mondiale était de 34,3 millions de t de chromite, alors que pour l’Union européenne (Finlande) elle était de 1,19 million de t.
| Afrique du Sud | 20 000 |
Albanie, en 2018 |
1 143 |
|
| Kazakhstan | 4 780 |
Zimbabwe | 870 | |
| Inde | 4 060 |
Oman, en 2018 | 688 | |
| Finlande | 1 190 | Russie, en 2018 | 507 | |
| Turquie | 1 090 |
Brésil, en 2018 | 500 |
Source : IMFA et BGS
Les ressources en chromite de la Chine sont très faibles, avec en 2018, une production de 30 000 t.
Producteurs
En Afrique du Sud, toutes les sociétés minières exploitent le Complexe du Bushveld dans des mines ou récupèrent la chromite présente dans les terrils résultant de l’extraction des platinoïdes de la couche UG2. On estime, en 2017, qu’un quart de la production d’Afrique du Sud provient de l’exploitation de ces terrils.
- En Afrique du Sud :
- Glencore possède 79,5 % de Glencore-Merafe Chromium Venture avec, en 2019, une production totale de chromite, de 3,037 millions de t. Les mines sont situées :
- dans le lobe ouest du complexe du Bushveld, près de Rustenburg, pour celles de Waterval avec une capacité de production de 240 000 t/an de chromite et Kroondal, avec une capacité de 967 000 t/an ainsi que celles de Marikana, Klipfontein et Boshoek. Les réserves prouvées et probables sont, fin 2019, de 24,44 millions de t de minerai renfermant 30,0 % de Cr2O3.
- dans le lobe est du complexe du Bushveld, près de Steelpoort, pour les mines de Thorncliffe avec une capacité de 871 000 t/an, Helena avec une capacité de 814 000 t/an et Magareng avec 731 000 t/an. Les réserves prouvées et probables sont, fin 2019, de 33,3 millions de t de minerai contenant 33,3 % de Cr2O3.
- dans le lobe ouest du complexe du Bushveld, près de Rustenburg, pour celles de Waterval avec une capacité de production de 240 000 t/an de chromite et Kroondal, avec une capacité de 967 000 t/an ainsi que celles de Marikana, Klipfontein et Boshoek. Les réserves prouvées et probables sont, fin 2019, de 24,44 millions de t de minerai renfermant 30,0 % de Cr2O3.
- Samancor possède des mines dans 2 régions : Ouest (Rustenburg) et Est (Lydenburg), avec une production de 4 millions de t/an de minerai dont 70 % alimente les usines de ferrochrome de la société situées à Middelburg, Emalahleni, Steelpoort et Mooinooi. Le reste, environ 1 million de t/an, est exporté. Les mines de l’ouest sont souterraines avec Mooinooi et Millsell, celles de l’est sont souterraines (3) ou à ciel ouvert avec Doornbosch, Lannex, Tweefontein, Steelport. Le 1er novembre 2019, a repris les activités de Hernic Ferrochrome, qui était détenu à 50,975 % par Mitsubischi (Japon) et exploitait, dans le lobe ouest, les mines de Morula (souterraine) et Bokone (souterraine et à ciel ouvert) et produisait 1,5 million de t/an.
- Assore exploite la mine souterraine de Dwarsrivier, avec, en 2019-20, une production de 1,551 million de t. Les réserves prouvées et probables sont de 58,89 millions de t de minerai renfermant 32,82 % de Cr2O3.
- African Rainbow Minerals, coproduit de la chromite lors de l’extraction de platinoïdes avec, en 2019, 442 494 t pour la mine de Nkomati détenue à 50 % en association avec Norilsk et 219 560 t pour la mine de Two Rivers détenue à 54 % en association avec Impala Platinium.
- Le groupe finlandais Afarak, exploite les mines de Vlakpoort, Mecklenburg et Stellite. En 2019, la production a été de 357 557 t de chromite. Les réserves prouvées et probables sont de 21,735 millions de t renfermant 35,32 % de Cr2O3.
- Glencore possède 79,5 % de Glencore-Merafe Chromium Venture avec, en 2019, une production totale de chromite, de 3,037 millions de t. Les mines sont situées :
- Au Kazakhstan :
- la production est assurée, en partie, par Eurasian Resources Group (ERG), avec une production, en 2018, de 5,6 millions de t de chromite avec la mine de Donskoy,
- ainsi que par le groupe turc Yildirim, avec la mine souterraine de Voskhod, près de Chromtau, dans la région d’Aktobe, avec une capacité de production de 1,3 million de t/an et des réserves de 20 millions de t de minerai, le minerai approvisionnant l’usine russe de production de ferrochrome de Tikhvin, à 200 km au sud-est de Saint-Pétersbourg. En 2019, la production a été de 670 000 t.
- Le groupe turc Yildirim, exploite également des mines en Turquie au travers de la société Eti Krom. La capacité de production est de 1 million de t/an, la principale mine exploitée étant celle de Guleman, dans la région d’Elazig et les réserves prouvées et probables sont de 130 millions de t. En 2019, la production a été de près de 800 000 t de chromite dont 700 130 t de teneur comprise entre 28 et 46 % et 99 440 t de teneur comprise entre 11 et 28 %.
- En Inde, les mines sont exploitées à 97 % dans la vallée de Sukinda, située dans l’État d’Orissa :
- Indian Metals & Ferro Alloys Ltd (IMFA), possède les mines de Mahagiri et de Sukinda ainsi que la mine en cours d’extension de Nuasahi, avec, en 2019-20, une production de 516 621 t de chromite et des réserves de 21 millions de t de minerai.
- Balasore Alloys Limited exploite une mine dans la vallée de Sukinda.
- En Finlande, une chromite, à 35 % de Cr2O3, est extraite de la mine de Kemi située en Laponie et exploité par Outokumpu. Le gisement, stratiforme, s’étend sur 15 km de long et entre 0,2 et 2 km de large, sur une épaisseur de 2 km. La mine, découverte en 1959, est exploitée à ciel ouvert depuis 1968 et souterrainement depuis 2003, avec une capacité de production de 2,4 millions de t/an. Les réserves prouvées sont, en 2015, de 48 millions de t à 26 % de Cr2O3.
Commerce international
Exportations
Les exportations représentaient, en 2019, un total de 19,466 millions de t de minerais et concentrés.
| Afrique du Sud | 14 860 | Pakistan | 335 | |
| Turquie | 1 316 | Albanie | 306 | |
| Kazakhstan | 699 | Pays Bas | 132 | |
| Oman | 593 | Papouasie | 131 | |
| Zimbabwe | 581 | Iran | 122 |
Source : ITC
Les exportations de l’Afrique du Sud sont destinées à 55 % à la Chine.
Importations
Les importations représentaient, en 2019, un total de 18,212 millions de t de minerais et concentrés.
| Chine | 15 921 | Allemagne | 151 | |
| Russie | 903 | Inde | 134 | |
| Indonésie | 445 | Japon | 56 | |
| Turquie | 177 | Belgique | 46 | |
| États-Unis | 152 | Autriche | 27 |
Source : ITC
Les importations de la Chine proviennent à 79 % d’Afrique du Sud, 6 % de Turquie, 4 % du Zimbabwe, 4 % d’Oman.
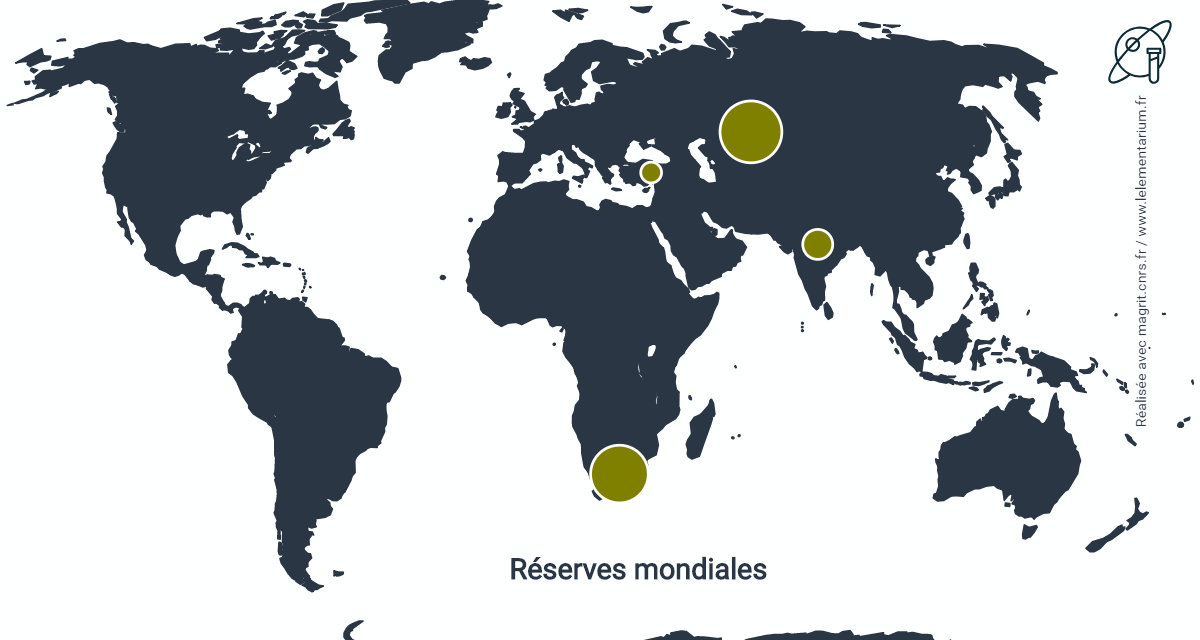
Réserves
Elles étaient estimées, en 2019, à 570 millions de tonnes de chromite :
| Kazakhstan | 230 000 | Inde | 100 000 | |
| Afrique du Sud | 200 000 | Turquie | 26 000 |
Source : USGS
Utilisations de la chromite : en 2017.
| Sidérurgie | 90 % | Fonderie | 2 % | |
| Chimie | 5 % | Réfractaires | 1 % |
Source : Roskill
- La chromite est, à 90 %, transformée en ferrochrome, lui même utilisé à 77 % pour l’élaboration d’aciers inoxydables, pour lesquels il est irremplaçable.
- Pour l’élaboration de produits chimiques la chromite est d’abord transformée en dichromate de sodium, Na2Cr2O7.
- En fonderie, la chromite est utilisée comme « sable » de confection de moules. Sa température de fusion est de 2 150°C.
- Pour une utilisation comme produit réfractaire, la somme des teneurs en Cr2O3 et Al2O3 doit être supérieure à 57 %, avec une teneur en silice inférieure à 0,7 %.
Métallurgie
La chromite est principalement transformée en ferrochromes. La transformation en chrome ne concerne qu’une très faible part de l’utilisation de la chromite.
Ferrochromes
Ils contiennent de 50 à 65 % de chrome et sont élaborés par réduction au four électrique à arc, en présence de coke. La consommation électrique est comprise entre 2 900 et 4 100 kWh/t de ferrochrome.
Principaux types de ferrochrome
Ils se distinguent principalement par leur teneur en carbone.
- Charge-chrome : 50 à 55 % de Cr, 6 à 8 % de C, 2 à 5 % de Si. C’est l’alliage de chrome le plus utilisé dans la fabrication des aciers spéciaux, dont les aciers inoxydables.
- Le ferrochrome carburé : 60 à 65 % de Cr, 4 à 8 % de C. Il est utilisé principalement dans l’élaboration des aciers inoxydables.
- Le ferrochrome moyen carbone : 55 à 70 % de Cr, de 2 à 4 % de C. Il représente 2 % de la production mondiale de ferrochrome.
- Le ferrochrome bas carbone affiné et suraffiné : 67 à 75 % de Cr, 0,02 à 0,5 % de C, est employé dans la fabrication de la fonte et des aciers. Il représente 4 % de la production mondiale de ferrochrome.
Le ferrochrome carburé et la charge chrome représentent, en 2014, 94 % de la production mondiale de ferrochrome.
Productions de ferrochrome
En 2019, la production mondiale de ferrochrome s’élevait à 14,73 millions de t.
L’Union européenne (Finlande, Suède, Allemagne) en produisait, en 2018, 620 000 t.
| Chine | 6 580 | Finlande |
510 | |
| Afrique du Sud | 4 780 | Russie, en 2018 |
332 | |
| Kazakhstan | 1 600 | Zimbabwe, en 2018 | 316 | |
| Inde | 1 280 | Brésil, en 2018 | 175 |
Sources : IMFA et BGS
La Chine est devenue premier producteur mondial de ferrochrome en 2012. De plus, en 2018, la Chine a importé 2,432 millions de t de ferrochrome possédant une teneur en carbone supérieure à 4 % dont 1,381 million de t d’Afrique du Sud. La production est principalement réalisée en Mongolie Intérieure avec, en 2018, 2,82 millions de t soit 53 % de la production totale du pays.
La production d’Afrique du Sud, qui pourrait être plus importante, souffre de difficultés d’approvisionnement en énergie électrique. En 2018, les exportations de l’Afrique du Sud ont été de 3,657 millions de t de ferrochrome possédant une teneur en carbone supérieure à 4 %.
En 2016, la production mondiale de charge-chrome est de 7,560 millions de t, celle de ferrochrome HC, de 3,552 millions de t.
Producteurs de ferrochrome
Les principaux producteurs mondiaux sont, en 2019, les suivants :
| Glencore-Merafe (Afrique du Sud) | 1 438 | Tianjin Metallurgy (Chine), en 2014 |
400 | |
| ERG (Kazakhstan, Russie), en 2014 | 1 200 | EHUI Metallurgy (Chine) |
400 | |
| Samancor (Afrique du Sud), en 2014 |
1 150 | Yildirim (Turquie, Russie, Suède) | 262 | |
| Outokumpu (Finlande) |
505 |
Source : Merafe et rapports des sociétés
- Glencore a produit, en 2019, en Afrique du Sud, 1,438 million de t de ferrochrome dans les usines de Wonderkop, avec une capacité de production de 553 000 t/an, Rustenburg, avec 430 000 t/an, Boshoek, avec 240 000 t/an, ces usines étant alimentées par les mines de Kroondal, Waterval et Marikana ainsi que dans les usines de Lydenburg, avec 396 000 t/an et Steelpoort (Lion I et II, avec 360 000 t/an chaque), alimentées par les mines de Thorncliffe, Helena et Marareng. L’autre partenaire de la joint-venture, Merafe, a produit, en 2019, 371 000 t de ferrochrome.
- Eurasian Resources Group (ERG) a produit, en 2012, 1,2 million de t de ferrochrome carburé, 91 000 t de ferrochrome bas carbone, 47 000 t de ferrochrome moyennement carburé et 185 000 t de ferrosilicochrome. La production est réalisée au Kazakhstan avec les usines de Kazchrome à Aktobe et Asku avec des capacités de production de 790 000 t/an de ferrochrome carburé et 109 000 t de ferrosilicochrome et en Russie, à Serov, région de Sverdlovsk, avec des ferrochromes carburé, moyen et bas carbone et du ferrosilicochrome.
- Samancor possède des capacités de production, en Afrique du Sud, de 1 million de t/an de charge-chrome, 70 000 t/an de ferrochrome moyennement carburé et 40 000 t/an de ferrochrome bas carbone, dans ses usines de Emalahleni, Middelburg, Steelport et Mooinooi. A acquis, en novembre 2019, Hernic Ferrochrome qui possède des capacités de production, en Afrique du Sud, de 420 000 t/an de charge-chrome à Maroelabult.
- Outokumpu a produit, à Tornio, en Finlande, en 2019, 505 000 t de ferrochrome, à partir de chromite extraite à Kemi, mine proche de Tornio.
- Le groupe turc Yildirim a produit, en 2019, 261 600 t de ferrochrome HC, en Turquie, à Elazig, avec 87 200 t, au travers de la société Eti Krom, en Russie au travers de Tikhvin Ferroalloys (TFZ) avec 56 300 t et en Suède, au travers de la société Vargön Alloys avec 119 900 t.
- Indian Metals & Ferro Alloys Ltd (IMFA) possède, en Inde, dans l’État d’Orissa, à Therubali et Choudwar, des capacités de production de 284 000 t/an de ferrochrome carburé et, en 2019-20, a produit 237 812 t de ferrochrome.
Chrome métal
Fabriqué par aluminothermie à partir d’oxyde de chrome (procédé employé en Chine, France, Russie et Royaume Uni et couvrant 70 % des besoins) ou par électrolyse à partir de ferrochrome (procédé utilisé en Russie et couvrant 30 % des besoins).
Par aluminothermie, la réaction mise en jeu est la suivante :
Cr2O3 + 2 Al = 2 Cr + Al2O3
L’oxyde de chrome doit être chimiquement pur. La réaction bien que fortement exothermique, n’apporte pas suffisamment d’énergie pour que les produits formés, réfractaires, se séparent correctement, par décantation, à l’état liquide. Pour élever la température, une partie de Cr2O3 est remplacée par un composé de degré d’oxydation plus élevé (CrO3 ou mieux, contenant des ions Cr2O72-). De 10 à 15 t de produit sont traitées à chaque opération.
Au laboratoire, le chrome peut être préparé par aluminothermie dans des conditions proches de celles utilisées industriellement en prenant un mélange de 60 g de dichromate de potassium et de 200 g d’oxyde de chrome (Cr2O3) pour 90 g d’aluminium (de granulométrie < 200 micromètres), introduit dans un creuset en alumine. Cette préparation nécessite de prendre des précautions face aux projections incandescentes et au risque toxique des poussières de chrome VI.
Le chrome obtenu par aluminothermie, malgré sa pureté élevée (99,5 à 99,8 %) n’est pas malléable même à 900°C. Il faut le purifier à l’aide de procédés tels que la méthode Van Arkel ou la fusion de zone pour obtenir du chrome laminable à 50-80 % vers 500°C. Dans ce cas, la transition ductile-fragile (fonction de la pureté) peut être proche de la température ambiante.
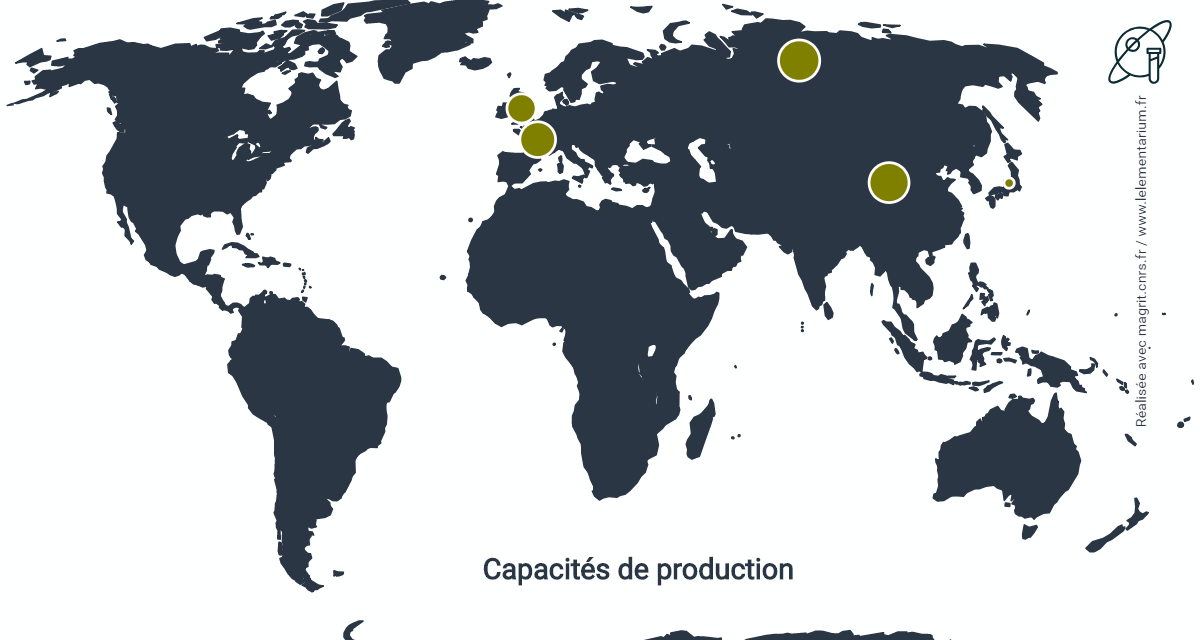
Capacités de production
En 2017, la capacité de production mondiale de chrome métal était de 57 000 t/an et de 21 000 t/an pour l’Union européenne.
| Russie | 19 | Royaume Uni | 8 | |
| Chine | 16 | Japon | 1 | |
| France | 12 | Allemagne | 1 |
Source : USGS
Les importations des États-Unis, ont été, en 2017, de 14 500 t.
Producteurs :
- Delachaux, avec sa filiale DCX Chrome (France), et une capacité de production par aluminothermie de 12 000 t/an à Marly-lez-Valenciennes (59).
- Kluchevsky Ferroalliages (Russie), filiale du groupe Midural, avec une capacité de production, par aluminothermie, de 10 000 t, à Dvurechensk, dans la région de Sverdlovsk.
- Polema, filiale du groupe Industrial Metallurgical Holding (Russie) par électrolyse à Tula.
- AMG Superalloys UK (Royaume-Uni) avec une capacité de production, par aluminothermie, de 8 000 t/an à Rotherham, au Royaume Uni.
- Japan Metals & Chemicals (JMC, Japon) produit par électrolyse à Research Triangle Park, en Caroline du Nord (États Unis) et à Oguni (Japon).
Produits chimiques
Le principal produit chimique élaboré est le dichromate de sodium Na2Cr2O7. Sa fabrication est effectuée dans un four tournant, vers 1 000°C, à partir d’un mélange de chromite et de carbonate de sodium qui donne du chromate de sodium selon la réaction :
2 Cr2O3 + 4 Na2CO3 + 3 O2 = 4 Na2CrO4 + 4 CO2
Le chromate de sodium soluble dans l’eau chaude donne, par acidification à l’aide d’acide sulfurique, du dichromate qui est cristallisé ensuite sous forme dihydratée.
Les différents autres composés chimiques du chrome (dichromates d’ammonium ou de potassium, oxydes, sulfate, acide chromique…) sont obtenus à partir du dichromate de sodium.
Capacités de production
En 2017, la capacité mondiale de production s’élevait à 334 000 t/an de chrome contenu dans des produits chimiques.
| Chine | 113 | Turquie | 28 | |
| États-Unis | 42 | Afrique du Sud | 18 | |
| Kazakhstan | 38 | Argentine | 12 | |
| Russie | 31 | Pologne | 7 | |
| Inde | 30 | Italie | 5 |
Source : USGS
En 2012, la production mondiale de dichromate de sodium était de 700 000 t.
Producteurs
Les principaux producteurs sont :
- Chongqing Minfeng Chemical Co., Ltd., en Chine.
- Elementis Chromium, aux États Unis, à Castle Hayne, en Caroline du Nord et Corpus Christi, au Texas.
- JS Aktyubinsk Chromium Chemicals Plant (ACCP), à Aktobe, au Kazakhstan.
- Russian Chrome Chemicals 1915, filiale du groupe Midural.
- Lanxess, en Afrique du Sud, extrait de la chromite à Rustenburg qui est transformée en dichromate de sodium et acide chromique à Newcastle puis en sulfate et sels de tannage à Merebank, près de Durban, avec une production de 64 000 t/an. Le dichromate de sodium fabriqué à Newcastle est transformé en pigments à Krefeld-Uerdingen, en Allemagne. En août 2019, cette activité a été vendue au groupe chinois Brother Enterprise.
- Sisecam, en Turquie, à Mersin et en Italie avec la société Cromital, à Ostellatto, dans la province de Ferrara. La capacité de production est de 128 000 t/an de sulfate de chrome.
Recyclage
Le chrome contenu dans les aciers inoxydables est recyclé lors du recyclage de ces matériaux. De même pour le chrome contenu dans les aciers courants. Le taux de recyclage du chrome, dans le monde, est estimé à 38 %. Ce taux était de 29 %, en 2019, aux États Unis, avec un recyclage de 140 000 t de chrome.
En France, la société Befesa Valera traite, à Gravelines (59), dans 2 fours à arc immergé, des poussières d’aciéries inoxydables et des déchets d’aciers inoxydables afin de récupérer le nickel et le chrome contenu, avec une capacité de traitement de 120 000 t/an d’acier inoxydable. Les déchets sont conditionnés sous forme de briquettes qui, additionnées de coke et de scorifiants sont introduites dans les fours d’où des coulées sont effectuées plusieurs fois par jour. Ce groupe possède également une usine du même type à Landskrona, en Suède, avec une capacité de traitement de 65 000 t/an d’acier inoxydable.
Situation française
En 2019.
Minerai
En 2019, il n’y a pas de production française. Une production, terminée en 1991, a eu lieu en Nouvelle Calédonie avec 60 000 t de minerai en 1989.
- Exportations : 4 779 t principalement vers :
- l’Espagne à 29 %,
- la Belgique à 17 %,
- l’Allemagne à 15 %,
- le Royaume Uni à 11 %,
- la Pologne à 10 %.
- Importations : 13 292 t en provenance :
- d’Afrique du Sud à 62 %,
- d’Albanie à 21 %,
- d’Allemagne à 5 %.
Ferrochrome
Pas de production en 2019.
Carburé et charge-chrome
- Exportations : 345 t vers :
- le Portugal à 30 %,
- l’Espagne à 12 %,
- l’Allemagne à 10 %,
- l’Italie à 8 %.
- Importations : 56 891 t en provenance :
- d’Afrique du Sud à 36 %,
- du Kazakhstan à 18 %,
- de Finlande à 15 %,
- de Suède à 9 %.
Moyennement carburé
- Exportations : 32 t vers :
- la Belgique à 52 %,
- l’Allemagne à 31 %.
- Importations : 1 838 t en provenance :
- de Russie à 94 %.
- de Russie à 94 %.
Bas carbone
- Exportations : 328 t vers :
- l’Allemagne à 32 %,
- la Suisse à 13 %,
- les Pays Bas à 9 %,
- l’Italie à 9 %.
- Importations : 4 755 t en provenance :
- de Russie à 41 %,
- de Turquie à 16 %,
- d’Allemagne à 14 %,
- de Belgique à 14 %.
Chrome Métal
Producteur :
Delachaux, à Marly-lez-Valenciennes (59), possède une capacité de la production 12 000 t/an. C’est le premier producteur européen de chrome métal par aluminothermie, le 3ème mondial. La production est à 90 % exportée.
- Exportations : 8 515 t vers :
- les États Unis à 33 %,
- l’Allemagne à 15 %,
- le Japon à 12 %,
- le Royaume Uni à 8 %.
- Importations : 295 t en provenance :
- de Russie à 53 %,
- du Royaume-Uni à 37 %,
- d’Allemagne à 7 %.
Produits chimiques
Trioxyde de chrome
- Exportations : 573 t vers :
- les États-Unis à 64 %,
- l’Italie à 9 %.
- Importations : 1 375 t en provenance :
- d’Allemagne à 54 %,
- de Turquie à 15 %,
- des États Unis à 12 %,
- d’Afrique du Sud à 7 %.
Dichromate de sodium
- Exportations : 32 t vers :
- la Belgique à 23 %,
- la Tunisie à 20 %,
- l’Équateur à 16 %,
- l’Espagne à 9 %.
- Importations : 1 235 t en provenance :
- d’Afrique du Sud à 55 %,
- d’Italie à 38 %.
Utilisations
Consommations
En 2015, la consommation mondiale de chromite a été de 29 millions de t.
En 2019, la consommation de ferrochrome a été de 13,7 millions de t répartie comme suit :
- 64,2 % en Chine,
- 9,0 % en Europe de l’Ouest,
- 4,8 % au Japon,
- 3,8 % aux États-Unis.
Secteurs d’utilisation
Les principaux secteurs utilisateurs, en 2018, dans le monde étaient les suivants :
| Sidérurgie | 90 % | Fonderie | 2 % | |
| Chimie | 5 % | Réfractaires | 1 % |
Source : Roskill
En sidérurgie, l’emploi dans les aciers inoxydables représente 77 % des utilisations, dans les aciers alliés : 19 %, dans les autres aciers : 4 %.
En fonderie, la chromite est employée comme « sable de moulage ».
Ferrochrome
Il est utilisé à 80 % pour l’élaboration d’aciers inoxydables, pour lesquels il est irremplaçable.
Métal
La répartition des utilisations en France est la suivante :
| Superalliages | 52 % | Autres alliages | 10 % | |
| Alliages d’aluminium | 12 % | Résistance électrique | 6 % | |
| Soudage et revêtement | 12 % | Autres | 8 % |
Composés chimiques
Le principal composé chimique utilisé est le dichromate de sodium Na2Cr2O7, qui entre dans la composition des produits de protection du bois (en présence d’arsenic, voir ce chapitre), des colorants de textiles, dans la fabrication de pigments minéraux. Le dichromate de potassium K2Cr2O7 est utilisé en photographie argentique, pyrotechnie, gravure de lithographie, colorant de céramiques. Le dichromate d’ammonium (NH4)2Cr2O7 donne par calcination le dioxyde de chrome CrO2 pour bandes magnétiques vidéo et audio et est utilisé comme agent oxydant dans des synthèses organiques.
L’acide chromique CrO3 entre dans la fabrication de catalyseurs, de pigments minéraux, permet le mordançage des textiles, le chromage dur et décor.
Le sulfate de chrome Cr2SO4 est employé dans le tannage du cuir.
Le trioxyde de chrome Cr2O3 est utilisé pour élaborer le chrome métal, des produits réfractaires, des pigments.
Principaux secteurs d’utilisation des produits chimiques, en 2015, étaient :
| Tannage du cuir | 27 % | Chromage | 19 % | |
| Chrome métal | 22 % | Protection du bois | 9 % | |
| Pigments | 19 % |
Source : ICDA
Chromage : on distingue le chrome décor du chrome dur.
- Chrome décor : le dépôt de chrome est effectué, par électrolyse, sous faible épaisseur (généralement de 0,2-0,3 micromètres), pour recouvrir des pièces métalliques qui sont essentiellement nickelées (voir le chapitre nickel). La couche finale de chrome n’a qu’un rôle esthétique, il permet d’éviter le ternissement de la surface de nickel par sulfuration.
- Chrome dur : le dépôt de chrome est effectué, par électrolyse, sous forte épaisseur (de plusieurs micromètres à quelques dixièmes de mm), directement sur la pièce à protéger. Le revêtement de chrome apporte une excellente résistance à l’usure, aux frottements, à la corrosion, une grande dureté de surface et des propriétés antiadhérentes. Utilisé pour de nombreuses pièces mécaniques en automobile (vilebrequins, chemises de cylindres…), aéronautique (pièces de réacteurs…), machines-outils (arbres de transmission…), outils (instruments de mesure…), moules pour plastiques…
Conditions de chromage : par électrolyse, vers 50-60°C, la pièce à revêtir étant placée à la cathode. L’anode est en alliage de Pb (7 % de Sb) et la densité de courant de 40 à 50 A/dm2. Composition du bain : CrO3 : 250 g/L, H2SO4 : 2,5 g/L, vitesse de dépôt : environ 40 micromètres/h.
Toxicité
D’après les fiches de l’INERIS et de l’INRS.
Les principaux composés courants du chrome présentant une toxicité élevée sont ceux des degrés d’oxydation III et VI. La voie de pénétration principale dans l’organisme est la voie respiratoire avec passage dans la circulation sanguine de 20 à 30 % du Cr (VI) inhalé. Ce taux est de 2 à 9 % par voie orale et de 1 à 4 % par voie cutanée. Les composés de chrome, oxydants puissants, ont une forte action corrosive se traduisant par des atrophies, ulcérations et perforations de la cloison nasale ainsi que par une diminution des fonctions pulmonaires et des pneumonies. Les composés de chrome VI plus solubles que les composés de chrome III sont plus facilement absorbés. Ils diffusent rapidement à travers les membranes et détruisent ainsi les cellules épithéliales.
Dans l’organisme, le chrome VI est réduit en chrome III, sa demie-vie étant de 15 à 41 h. Au cours de sa réduction des composés très réactifs, par exemple de chrome V, peuvent être produits. Toutefois, le Cr(III), à l’état de trace, est nécessaire à l’organisme humain, en particulier pour le métabolisme du cholestérol, des graisses et du glucose. Une carence en chrome induit des hyperglycémies et des hypercholestérolémies.
Par ailleurs, les composés de chrome III et VI sont mutagènes et cancérogènes (cancers du poumon). Après solubilisation dans l’organisme, un effet sensibilisant se traduit par de l’asthme ou des dermatites.
En milieu professionnel, la valeur moyenne limite d’exposition est de 0,05 mg/m3. La teneur limite des eaux de consommation est, en chrome total, de 50 microgrammes/L.
Bibliographie