Données physico-chimiques
Données atomiques
| Numéro atomique | Masse atomique | Configuration électronique | Structure cristalline |
| 112 | 285 g.mol-1 | [Rn] 7s2 5f14 6d10 | Cubique centrée |
Données physiques
| Masse volumique |
| 23,7 g.cm-3 |
| Numéro atomique | Masse atomique | Configuration électronique | Structure cristalline |
| 112 | 285 g.mol-1 | [Rn] 7s2 5f14 6d10 | Cubique centrée |
| Masse volumique |
| 23,7 g.cm-3 |
| Numéro atomique | Masse atomique | Configuration électronique | Structure cristalline |
| 111 | 282 g.mol-1 | [Rn] 7s2 5f14 6d9 | Cubique centrée |
| Masse volumique |
| 28,7 g.cm-3 |
| Formule | Géométrie | Nom UICPA | Masse molaire |
| C2H3Cl3 | 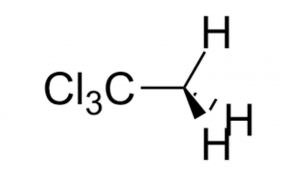 |
1,1,1-trichloroéthane | 133,40 g.mol-1 |
| Masse volumique | Température de fusion | Température d’ébullition | Température d’auto-inflammation | Limites d’explosivité dans l’air | Solubilité dans l’eau |
| liquide, 20°C, 101,3 kPa : 1,32 g.cm-3 | -33°C | 74°C | 537°C | Entre 8 et 10,5 % en volume | à 20°C : 0,480 g/L |
| Valeur limite d’exposition | Valeur moyenne d’exposition | ||
| ppm | mg/m3 | ppm | mg/m3 |
| 200 | 1 100 | 100 | 555 |
Le trichloro-1,1,1 éthane est également appelé méthylchloroforme.
Voir également le produit solvants chlorés.
Voir le produit solvants chlorés.
Il peut être stabilisé avec des teneurs inférieures à 5 % par divers produits : 1,4 dioxanne, oxyde de 1,2-butylène, nitroalcanes, 2-méthyl-2-propanol…
Producteurs
Consommations : répartition de la consommation, en 2017 :
| États-Unis | 65 % | Europe de l’Ouest | 35 % |
Source : IHS Markit
Secteurs d’utilisation : jusqu’en 1996, principalement dans le dégraissage des métaux. Il a eu tendance, avant son interdiction, à remplacer le trichloréthylène. Actuellement, il est principalement employé comme intermédiaire dans la production de polymères fluorés comme le polyfluorure de vinylidène.
Avant 1996, il fût utilisé dans le blanc correcteur.
Évolution des utilisations dans le dégraissage des métaux :
L’interdiction du trichloro-1,1,1 éthane s’est traduite par le développement d’autres moyens de dégraissage à l’aide de lessives en milieu aqueux ou d’hydrocarbures (par exemple du type White-spirit). Le trichloro-1,1,1 éthane avait, en partie, remplacé le trichloréthylène, toxique (en 2002, il était passé de la catégorie 3 des substances cancérogènes à la catégorie 2 « peut causer le cancer » avec une phrase de risque R45 et en 2012, à la catégorie 1B « substance que l’on sait être cancérogène pour l’homme »).
L’interdiction du trichloro-1,1,1 éthane se traduit, dans le cas de dégraissages méticuleux de pièces pour lesquelles les produits lessiviels ne conviennent pas, par le retour à l’emploi du trichloréthylène. Au Japon, le trichloro-1,1,1 éthane est remplacé par le chlorure de méthylène.
Le trichloro-1,1,1 éthane, qui a un temps de demi-vie dans l’atmosphère de 3,7 ans est concerné par le Protocole de Montréal destiné à préserver la couche d’ozone. Son utilisation comme solvant est interdite depuis le 1er janvier 1996. Dans l’Union européenne, sa production et son importation sont interdites mais toutefois, par dérogation après autorisation, son utilisation comme intermédiaire dans la fabrication de divers produits chimiques tels que les HFA 141 et 142b est possible.
L’exposition chronique aux vapeurs de trichlo-1,1,1-éthane est à l’origine d’irritations cutanée, oculaire et respiratoire.
Les phrases de danger associées au trichloro-1,1,1 éthane sont les suivantes :
H332 – Nocif par inhalation,
H420 – Nuit à la santé publique et à l’environnement en détruisant l’ozone dans la haute atmosphère.
| Formule | Géométrie | Nom UICPA | Masse molaire |
| C2Cl4 | 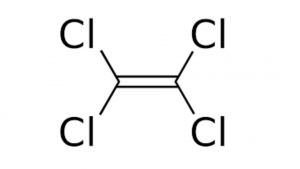 |
Tétrachloroéthène | 165,83 g.mol-1 |
| Masse volumique | Température de fusion | Température d’ébullition | Solubilité dans l’eau |
| liquide, 20°C, 101,3 kPa : 1,60 g.cm-3 | -22°C | 121,2°C | à 20°C : 0,15 g/L |
| Valeur limite d’exposition | Valeur moyenne d’exposition | ||
| ppm | mg/m3 | ppm | mg/m3 |
| 40 | 275 | 20 | 138 |
Voir également le produit solvants chlorés.
Voir le produit solvants chlorés.
Dans l’Union européenne, en 2018, la production de trichloréthylène et de perchloréthylène de 135 328 t.
Commerce international : en 2019.
Principaux pays exportateurs sur un total mondial de 155 768 t.
| Allemagne | 60 669 | République tchèque | 9 474 | |
| France | 23 386 | Inde | 7 117 | |
| États-Unis | 22 194 | Japon | 6 004 | |
| Belgique | 12 665 | Pays Bas | 5 790 |
Source : ITC
Les exportations allemandes sont destinées à 60 % à la Chine, 12 % à l’Italie, 5 % à la Russie.
Principaux pays importateurs sur un total mondial de 152 411 t.
| Chine | 51 535 | Turquie | 6 736 | |
| Belgique | 10 719 | Russie | 6 695 | |
| Inde | 8 326 | Pays Bas | 5 321 | |
| Italie | 7 934 | Royaume Uni | 4 500 |
Source : ITC
Les importations chinoises proviennent à 79 % d’Allemagne, 18 % des États-Unis, 2 % du Japon.
Principaux producteurs : voir le produit solvants chlorés.
Producteur :
Commerce extérieur : en 2019.
Consommations : répartition de la consommation, en 2017 :
| Chine | 40 % | Europe de l’Ouest | 9 % | |
| États-Unis | 37 % |
Source : IHS Markit
Secteurs d’utilisation : principalement dans le nettoyage à sec des vêtements.
Autres utilisations :
Historique du nettoyage à sec et évolution des utilisations : d’après Le pressing, nettoyage à sec ou aquanettoyage, document INRS.
Le nettoyage à sec trouva son origine en France au début du XIXème siècle, quand M. Jolly renversa le contenu d’une lampe à pétrole sur une nappe tachée : les taches disparurent une fois la nappe séchée. Fort de cette expérience, il fit ouvrir le premier établissement de nettoyage à sec en 1855 à Paris. Jusqu’en 1897, les produits employés furent hautement inflammables et toxiques (essence, pétrole, benzène). Au début du XXème siècle apparut le tétrachlorure de carbone, moins inflammable mais toxique, qui fut remplacé par le trichloréthylène dans les années 1920 en Europe. Après la Seconde Guerre mondiale, le perchloroéthylène commence à se substituer au trichloréthylène en raison de sa moindre toxicité ; le trichloréthylène ayant totalement disparu de la profession dans les années soixante. À partir de 2010, le perchloroéthylène commence à être remplacé par des solutions de nettoyage aqueux (aqua-nettoyage), ou d’autres solvants organiques alternatifs.
Dans le nettoyage à sec qui consommait principalement du perchloréthylène. En France, en 2013, fonctionnaient 5 200 machines de nettoyage à sec (2 300 en 2017) dont 93 % utilisaient du perchloréthylène et étaient situées dans des locaux contigus à des locaux occupés par des tiers.
En 1975, 90 % des solvants utilisés (32 000 t) partaient dans l’atmosphère. Les nouvelles machines mises sur le marché fonctionnent en circuit fermé et possédant un système interne de régénération du solvant, leur consommation est fortement réduite. La consommation est ainsi passée, par machine, de 3 t/an à 300 kg/an (1 L de perchloréthylène peut nettoyer 80 kg de vêtements).
En France, l’arrêté du 5 décembre 2012, paru au Journal Officiel du 9 décembre 2012, précise qu’à compter du 1er mars 2013, aucune nouvelle installation de machine de nettoyage à sec fonctionnant au perchloréthylène ne pourra être utilisée dans un local contigu à des locaux occupés par des tiers. Les machines déjà installées dans ce type de local seront progressivement interdites : celles mises en service avant 1999 seront interdites le 1er septembre 2014 et finalement toutes seront interdites à compter du 1er janvier 2022.
Les produits de substitution proposés sont : le nettoyage aqueux, l’éther tert-butylique du dipropylèneglycol, le dibutoxyméthane, les hydrocarbures en C9-C13, le décaméthylcyclopentasiloxane.
Voir le produit solvants chlorés.
Le perchloréthylène est absorbé à l’état gazeux par inhalation et à l’état liquide par la peau. Il a des répercussions sur le système nerveux et les reins. Un intoxication aiguë se manifeste essentiellement par la dépression du système nerveux central de type anesthésique.
Il est classé cancérogène possible (catégorie 3) par l’Union européenne et cancérogène probable (catégorie 2A) par l’International Agency for Research on Cancer (IARC).
Les phrases de danger associées au perchloréthylène sont les suivantes :
H351 – Susceptible de provoquer le cancer,
H411 – Toxique pour les organismes aquatiques, entraîne des effets néfastes à long terme.
| Formule | Géométrie | Nom UICPA | Masse molaire |
| C2HCl3 | 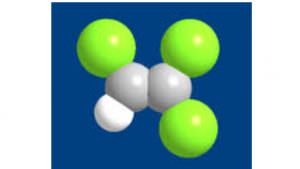 |
1,1,2-trichloroéthène | 131,39 g.mol-1 |
| Masse volumique | Température de fusion | Température d’ébullition | Température critique | Pression critique | Température d’auto-inflammation | Limites d’explosivité dans l’air | Solubilité dans l’eau |
| liquide, 20°C, 101,3 kPa : 1,280 g.cm-3 | -73°C | 87°C | 298,85°C | 5 050 kPa | 410°C | Entre 8 et 10,5 % en volume | à 20°C : 1 g/L |
| Valeur limite d’exposition | Valeur moyenne d’exposition | ||
| ppm | mg/m3 | ppm | mg/m3 |
| 200 | 1 080 | 75 | 405 |
Voir également le produit solvants chlorés.
Voir le produit solvants chlorés.
Le trichloréthylène, qui peut libérer du chlorure d’hydrogène, peut être stabilisé avec moins de 2 % d’un mélange d’amines, époxydes, dérivés du pyrrole…
En 2011, la capacité mondiale de production de trichloréthylène est de 547 000 t/an et la production de 429 500 t.
Dans l’Union européenne, en 2019, la production de trichloréthylène et de perchloréthylène de 96 476 t.
Commerce international : en 2019.
Principaux pays exportateurs sur un total mondial de 69 184 t.
| Chine | 31 607 | Japon | 9 891 | |
| États-Unis | 19 400 | Pays Bas | 6 326 |
Source : ITC
Les exportations chinoises sont destinées à 19 % à l’Inde, 12 % au Japon, 10 % à la Turquie.
Principaux pays importateurs sur un total mondial de 73 431 t.
| Pays Bas | 11 460 | Chine | 5 908 | |
| Allemagne | 9 275 | Russie | 4 102 | |
| Inde | 6 456 | Japon | 3 875 | |
| Corée du Sud | 6 095 | Turquie | 2 899 |
Source : ITC
Les importations des Pays Bas proviennent à 99 % des États-Unis.
Principaux producteurs : voir le produit solvants chlorés.
Commerce extérieur : en 2019.
Consommations : en 2011, la consommation mondiale est de 429 500 t. Répartition de la consommation, en 2017 :
| Chine | 58 % | Japon | 6 % | |
| États-Unis | 19 % | Europe de l’Ouest | 5 % |
Source : IHS Markit
En 2011, la consommation des États-Unis est de 116 000 t.
Secteurs d’utilisations : principalement comme intermédiaire chimique pour 80 % des utilisations, en 2010, dans l’Union européenne et à 20 % comme solvant, principalement dans le dégraissage des métaux, en phase vapeur.
Évolution des utilisations :
La consommation de trichloréthylène comme solvant était, dans l’Union européenne de 184 000 t en 1984. Cette utilisation représentait 75 % de la consommation. En 2006, elle a chuté à 25 000 t et, en 2010, à 10 000 t.
Dégraissage des métaux :
L’interdiction du trichloro-1,1,1 éthane s’est traduite par le développement d’autres moyens de dégraissage à l’aide de lessives en milieu aqueux ou d’hydrocarbures (par exemple du type White-spirit). Le trichloro-1,1,1 éthane avait, en partie, remplacé le trichloréthylène, toxique (en 2002, il était passé de la catégorie 3 des substances cancérogènes à la catégorie 2 « peut causer le cancer » avec une phrase de risque R45 et en 2012, à la catégorie 1B « substance que l’on sait être cancérogène pour l’homme »).
L’interdiction du trichloro-1,1,1 éthane se traduit, dans le cas de dégraissages méticuleux de pièces pour lesquelles les produits lessiviels ne conviennent pas, par le retour à l’emploi du trichloréthylène. Au Japon, le trichloro-1,1,1 éthane est remplacé par le chlorure de méthylène.
L’utilisation de machines de dégraissage fermées permet de diminuer, dans ce secteur, la consommation de trichloréthylène et les rejets dans l’atmosphère. Les consommations sont ainsi passées de 1 à 2 kg/h à moins de 100 g/h.
Le trichloréthylène est, dans l’Union européenne, interdit à la vente aux particuliers et est réservé, sous autorisation, à un emploi industriel.
Voir le produit solvants chlorés.
Le trichloréthylène n’est pas concerné par le Protocole de Montréal.
L’inhalation de fortes concentrations de trichloroéthylène, en particulier par des toxicomanes, provoque une dépression du système nerveux central pouvant aller jusqu’au coma. Lors d’ingestion apparaissent des troubles digestifs, neurologiques, cardiaques et respiratoires souvent graves. L’exposition répétée par inhalation peut provoquer des atteintes neuropsychiques parfois sérieuses. Une dermatose chronique est observée en cas de contacts répétés avec la peau.
Le trichloréthylène, considéré cancérogène de catégorie 1B par l’International Agency for Research on Cancer (IARC) depuis le 2012, est classé toxique.
Dans l’Union européenne, il ne peut être utilisé qu’après autorisation car il est inscrit à l’annexe XIV de REACH.
Il est interdit à la vente aux particuliers, dans l’Union européenne, lorsque sa présence dans un produit est supérieure à 0,1 %.
En France, les valeurs limite et moyenne d’exposition, respectivement de 200 et 75 ppm, sont particulièrement élevées. Le Scientific Committee on Occupational Exposure Limits (Scoel) recommande, depuis avril 2009, une valeur limite de 30 ppm (164 mg/m3) et une valeur moyenne d’exposition de 10 ppm (55 mg/m3).
Les phrases de danger associées au trichoréthylène sont les suivantes :
H350 – Peut provoquer le cancer,
H341 – Susceptible d’induire des anomalies génétiques,
H319 – Provoque une sévère irritation des yeux,
H315 – Provoque une irritation cutanée,
H336 – Peut provoquer somnolence ou vertiges,
H412 – Nocif pour les organismes aquatiques, entraîne des effets néfastes à long terme.
| Formule | Géométrie : tétraédrique | Nom UICPA | Masse molaire |
| CCl4 | 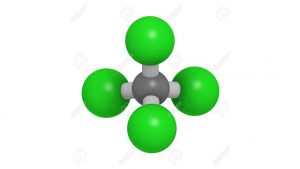 |
Tétrachlorométhane | 153,82 g.mol-1 |
| Masse volumique | Température de fusion | Température d’ébullition | Température critique | Pression critique | Température d’auto-inflammation | Solubilité dans l’eau |
| liquide, 0°C, 101,3 kPa : 1,594 g.cm-3 | -23°C | 76,7°C | 283,25°C | 4 560 kPa | 982°C | à 20°C : 800 mg/L |
| Valeur limite d’exposition | Valeur moyenne d’exposition | ||
| ppm | mg/m3 | ppm | mg/m3 |
| 10 | 60 | 2 | 12 |
Voir également le produit solvants chlorés.
Voir le produit solvants chlorés.
La production mondiale de tétrachlorure de carbone est, en 2014, de 202 700 t, à 39 % en Chine, 28 % aux États-Unis, 16 % dans l’Union européenne, 9 % en Inde, 5 % au Japon, 2 % en Corée du Sud. 163 700 t sont produites par chloration du méthane ou du chlorure de méthyle dans 35 usines dans le monde, 39 000 t sont coproduites lors de l’obtention du perchloréthylène dans 5 usines, 2 aux États-Unis et 3 dans l’Union européenne.
Dans l’Union européenne, en 2018, la production de tétrachlorure de carbone est de 23 755 t.
Commerce international : en 2019. Il obligatoirement faible car interdit par le Protocole de Montréal sauf, par dérogation, aux fins d’utilisations essentielles.
Principaux pays exportateurs sur un total de 6 549 t.
| Allemagne | 4 728 | États-Unis | 644 | |
| Chine | 1 151 | Pologne | 21 |
Source ITC
Les exportations allemandes sont destinées à 62 % à la France, 14 % aux États-Unis, 13 % au Royaume Uni.
Principaux pays importateurs sur un total de 13 869 t.
| États-Unis | 9 217 | Inde | 926 | |
| France | 2 923 | Japon | 553 |
Source : ITC
Les importations des États-Unis proviennent à 91 % de France, 9 % d’Allemagne.
Principaux producteurs : voir le produit solvants chlorés.
Production, en 2018 : confidentielle.
Producteurs :
Commerce extérieur :
Consommations : répartition de la consommation, en 2018.
| États-Unis | 47 % | Sous continent indien | 13 % | |
| Asie du Nord-Est | 29 % | Europe de l’Ouest | 12 % |
Source : IHS Markit
En 2015, la consommation des États-Unis est de 65 000 t.
Secteurs d’utilisation : répartition des utilisations, en 2014.
| Obtention du perchloréthylène | 32 % | Obtention du chlorure de méthyle | 13 % | |
| Obtention de HFC | 28 % | Obtention du tétrachlorobutyronitrile | 11 % |
Sources : Nolan Sherry & Associate et EMPA, SPARC Workshop, octobre 2015
Un partie de la production, 14 %, ne trouvant pas d’emploi, est incinérée.
Voir le produit solvants chlorés.
Protection de l’environnement : le tétrachlorure de carbone qui a un temps de vie dans l’atmosphère compris entre 36 et 58 ans et un potentiel d’appauvrissement de la couche d’ozone de 1,1, est concerné par le Protocole de Montréal destiné à préserver la couche d’ozone. Dans les pays développés il est interdit à la production et aux importations depuis le 1er janvier 1996 et pour les pays en développement, depuis le 1er janvier 2010. Toutefois des dérogations sont possibles aux fins d’utilisations essentielles.
En 2012, le tétrachlorure de carbone représente 12 % du chlore et du brome inorganiques participant à l’appauvrissement de la couche d’ozone.
Toxicité : absorbé par voies respiratoire, digestive ou par une peau lésée, il forme des métabolites toxiques au niveau hépatique.
En cas d’ingestion, les premiers signes de l’intoxication sont digestifs (nausées, vomissements, douleurs abdominales). Ils s’accompagnent ensuite d’une atteinte neurologique centrale (céphalées, sensations de vertige, somnolence, puis coma) ; les atteintes hépatique et rénale, qui font la gravité de l’intoxication, apparaissent 24 à 48 heures après la prise. La survenue d’un œdème aigu du poumon est fréquente.
Les phrases de danger suivantes sont associées au tétrachlorure de carbone :
H351 – Susceptible de provoquer le cancer,
H331 – Toxique par inhalation,
H311 – Toxique par contact cutané,
H301 – Toxique en cas d’ingestion,
H372 – Risque avéré d’effets graves pour les organes à la suite d’expositions répétées ou d’une exposition prolongée,
H412 – Nocif pour les organismes aquatiques, entraîne des effets néfastes à long terme,
H420 – Nuit à la santé publique et à l’environnement en détruisant l’ozone dans la haute atmosphère.
| Formule | Géométrie : tétraédrique | Nom UICPA | Masse molaire | Moment dipolaire |
| CHCl3 | 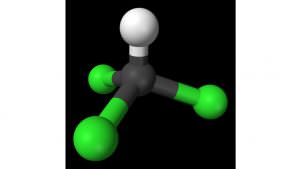 |
Trichlorométhane | 119,38 g.mol-1 | 1,15 D |
| Masse volumique | Température de fusion | Température d’ébullition | Température critique | Pression critique | Solubilité dans l’eau |
| liquide, 25°C, 101,3 kPa : 1,49 g.cm-3 | -63,5°C | 61,2°C | 263,25°C | 5 370 kPa | à 20°C : 8,09 g/L |
| Valeur limite moyenne d’exposition | |
| ppm | mg/m3 |
| 2 | 10 |
Voir également le produit solvants chlorés.
Du chloroforme est produit naturellement par des algues marines et des champignons. Ces émissions dans l’atmosphère sont estimées à 540 000 t/an.
Voir le produit solvants chlorés.
Le chloroforme pouvant s’oxyder lentement à l’air, en présence de lumière, pour donner du phosgène selon la réaction suivante :
2 CHCl3 + O2 = 2 COCl2 + 2 HCl
il peut être stabilisé par ajout de 0,75 % d’éthanol ou 0,006 % d’amylène.
Dans l’Union européenne, en 2019, la production de chloroforme est de 120 000 t dont 42 459 t en France, 21 667 t en Italie, la production allemande étant confidentielle.
Commerce international : en 2019.
Principaux pays exportateurs sur un total de 126 530 t.
| Allemagne | 43 933 | Corée du Sud | 11 712 | |
| États-Unis | 42 204 | Russie | 8 453 | |
| Chine | 14 232 | Taipei chinois | 3 935 |
Source : ITC
Les exportations allemandes sont destinées à 52 % aux Pays Bas, 18 % à l’Italie, 15 % à la France, 11 % à l’Inde.
Principaux pays importateurs :
| Inde | 54 252 | Pakistan | 7 469 | |
| Italie | 16 879 | Chine | 3 825 | |
| Japon | 14 641 | France | 3 732 | |
| Pays Bas | 10 078 | Iles Vierges | 3 725 |
Source ITC
Les importations indiennes proviennent à 42 % de Chine, 33 % des États-Unis, 8 % de Corée du Sud.
Principaux producteurs : voir le produit solvants chlorés.
Production, en 2019, de chloroforme : 42 459 t.
Producteurs :
Commerce extérieur : en 2019.
Consommations : répartition de la consommation, en 2018.
| Asie du Nord-Est | 60 % | Sous-continent indien | 12 % | |
| États-Unis | 13 % | Europe de l’Ouest | 11 % |
Source : IHS Markit
Secteurs d’utilisation :
Voir le produit solvants chlorés.
Du chloroforme peut être produit, en faible quantité par inadvertance, selon la réaction haloforme. Par exemple par action de l’eau de Javel sur de l’acétone ou de l’éthanol selon la réaction :
3 ClO– + (CH3)2CO = CHCl3 + 2 OH– + CH3COO–
L’intoxication aiguë par le chloroforme se traduit par des troubles neurologiques (confusion, coma) parfois associés à une dépression respiratoire. Des atteintes hépatiques et rénales sont également observées. Il est légèrement irritant pour la peau et fortement irritant pour les yeux.
L’inhalation chronique peut provoquer des troubles neurologiques, hépatiques et rénaux.
Les phrases de dangers associées au chloroforme sont les suivantes :
H302 – Nocif en cas d’ingestion,
H315 – Provoque une irritation cutanée,
H319 – Provoque une sévère irritation des yeux,
H331 – Toxique par inhalation,
H351 – Susceptible de provoquer le cancer,
H361d – Susceptible de nuire au fœtus,
H372 – Risque avéré d’effets graves pour les organes à la suite d’expositions répétées ou d’une exposition prolongée
| Formule | Géométrie : tétraédrique | Nom UICPA | Masse molaire | Moment dipolaire |
| CH2Cl2 | 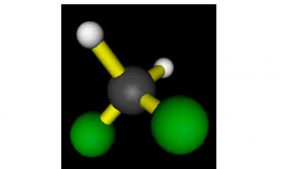 |
Dichlorométhane | 84,93 g.mol-1 | 1,14 D |
| Masse volumique | Température de fusion | Température d’ébullition | Température critique | Pression critique | Température d’auto-inflammation | Limites d’explosivité dans l’air | Solubilité dans l’eau |
| liquide, 20°C, 101,3 kPa : 1,33 g.cm-3 | -95,1°C | 40,1°C | 236,85°C | 6 300 kPa | 556°C | entre 12 et 25 % en volume | à 25°C : 17,5 g/L |
| Valeur limite d’exposition | Valeur moyenne d’exposition | ||
| ppm | mg/m3 | ppm | mg/m3 |
| 100 | 356 | 50 | 178 |
Voir également le produit solvants chlorés.
Voir le produit solvants chlorés.
Le chlorure de méthylène étant susceptible de se décomposer au dessus de 120°C, en chlorure d’hydrogène, phosgène…, des stabilisants (éthanol, méthanol, cyclohexane, composés phénoliques, amines, oxyde de propylène…), à des teneurs inférieures à 1 % peuvent être ajoutés.
En 2010, la production mondiale était de 814 000 t dans 26 unités de production.
Dans l’Union européenne, en 2019, la production de chlorure de méthylène est de 150 310 t dont 84 412 t en Allemagne, 41 411 t en France, 21 969 t en Italie, 2 483 t en Espagne.
Commerce international : en 2019.
Principaux pays exportateurs sur un total de 449 091 t.
| Chine | 186 356 | Taipei chinois | 16 064 | |
| Allemagne | 82 530 | Japon | 14 211 | |
| États-Unis | 47 542 | Russie | 12 668 | |
| France | 36 802 | Belgique | 7 892 | |
| Corée du Sud | 21 662 | Singapour | 4 940 |
Source : ITC
Les exportations chinoises sont destinées à 27 % à l’Inde, 10 % à la Corée du Sud, 6 % à la Turquie.
Principaux pays importateurs :
| Inde | 84 504 | Vietnam | 13 959 | |
| Turquie | 34 248 | Nigeria | 13 203 | |
| Corée du Sud | 27 140 | Italie | 12 886 | |
| Brésil | 16 172 | Royaume Uni | 12 393 | |
| Indonésie | 15 285 | Thaïlande | 11 918 |
Source : ITC
Les importations indiennes proviennent à 60 % de Chine, 10 % des Pays Bas, 9 % de la Corée du Sud.
Principaux producteurs : voir le produit solvants chlorés.
Productions : en 2019 : 41 411 t.
Producteurs :
Commerce extérieur : en 2019.
Consommations : répartition de la consommation, en 2018.
| Asie du Nord-Est | 57 % | États-Unis | 7 % | |
| Sous-contient indien | 11 % | Sud-Est asiatique | 5 % | |
| Europe de l’Ouest | 9 % | Moyen-Orient | 4 % |
Source : IHS Markit
En 2015, la consommation des États-Unis est de 119 737 t.
Secteurs d’utilisation : principalement comme solvant, dans le décapage des peintures et en pharmacie, car il dissout de très nombreuses substances et s’évapore très rapidement.
Voir le produit solvants chlorés.
La principale voie d’introduction du chlorure de méthylène chez l’homme est la voie respiratoire avec, comme cible principale, le système nerveux central, le foie et les poumons. Il est métabolisé en monoxyde et dioxyde de carbone, une intoxication pouvant être liée au monoxyde de carbone.
Le Centre International de Recherche sur le Cancer l’a classé en catégorie 2B, substance susceptible de provoquer un cancer.
L’Union européenne a, depuis décembre 2010, interdit son utilisation, par les consommateurs, dans les décapants pour peintures. L’Agence de protection de l’environnement des États-Unis a décidé son interdiction comme décapant de peintures pour usage grand public, à compter du 24 novembre 2019.
Le chlorure de méthylène n’est pas concerné par le Protocole de Montréal pour la protection de la couche d’ozone car, dans l’atmosphère, il est rapidement dégradé à la lumière, sa demie-vie étant inférieure à 6 mois.
| Formule | Géométrie : tétraédrique | Nom UICPA | Masse molaire | Moment dipolaire |
| CH3Cl | 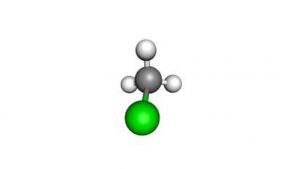 |
Chlorométhane | 50,49 g.mol-1 | 1,9 D |
| Masse volumique | Température de fusion | Température d’ébullition | Température critique | Pression critique | Température point triple | Pression point triple | Température d’auto-inflammation | Limites d’explosivité dans l’air | Solubilité dans l’eau |
| gazeux, 0°C, 101,3 kPa : 2,31.10-3 g.cm-3 | -97,6°C | -24,2°C | 143,1°C | 6 680 kPa | -97,72°C | 0,876 kPa | 632°C | entre 7,6 et 19 % en volume | à 25°C : 5 g/L |
| Valeur limite d’exposition | Valeur moyenne d’exposition | ||
| ppm | mg/m3 | ppm | mg/m3 |
| 100 | 210 | 50 | 105 |
Voir également le produit solvants chlorés.
Le chlorure de méthyle est produit naturellement par des algues marines et la décomposition du bois. Les quantités produites ainsi sont, dans le monde, considérables : de 3 à 8 millions de t/an.
Voir le produit solvants chlorés.
La production mondiale de chlorure de méthyle, en 2007, est d’environ 2 millions de t. Dans l’Union européenne, en 2019, la production de chlorures de méthyle et d’éthyle est de 300 000 t dont 229 796 t en Allemagne et 28 764 t en France, en 2017.
Commerce international : en 2019.
Principaux pays exportateurs sur un total de 109 995 t.
| Allemagne | 74 336 | Chine | 12 573 | |
| États-Unis | 14 863 | France | 5 501 |
Source : ITC
Les exportations allemandes sont destinées à 27 % au Royaume Uni, 20 % à la France, 20 % à la Belgique, 13 % à la Suède.
Principaux pays importateurs sur un total de 99 905 t.
| Royaume Uni | 25 430 | États-Unis | 4 035 | |
| France | 20 582 | Allemagne | 3 333 | |
| Belgique | 13 754 | Inde | 2 663 | |
| Suède | 9 044 | Brésil | 2 644 | |
| Italie | 7 070 | Canada | 2 175 |
Source : ITC
Les importations du Royaume Uni proviennent à 70 % d’Allemagne, 20 % des Pays Bas, 8 % des États-Unis.
Principaux producteurs : voir le produit solvants chlorés.
Production : en 2017 de chlorures de méthyle et d’éthyle : 28 764 t.
Producteurs :
Commerce extérieur : en 2019.
Consommations : répartition de la consommation, en 2018, sur un total mondial de 2 millions de t.
| Europe de l’Ouest | 37 % | États-Unis | 20 % | |
| Asie du Nord-Est | 35 % | Asie du Sud-Est | 4 % |
Source : IHS Markit
Le chlorure de méthyle représente, en 2016, 53 % de la consommation de chlorométhanes.
Secteurs d’utilisation : c’est un intermédiaire de synthèse de divers produits (c’est un agent de méthylation en synthèse organique). Répartition de la consommation mondiale, en 2016 :
| Silicones | 85 % | Herbicides | 2 % | |
| Méthylcellulose | 8 % | Caoutchouc butyle | 1 % | |
| Ammonium quaternaire | 3 % |
Source : IHS
Voir le produit solvants chlorés.
| Formule | Distance C-H | Masse molaire |
| CH4 | 108,70 pm | 16,04 g.mol-1 |
| Masse volumique | Température de fusion | Température d’ébullition | Température critique | Pression critique | Température point triple | Pression point triple | Température d’auto-inflammation | Limites d’explosivité dans l’air | Solubilité dans l’eau |
| gazeux, 15°C, 101,3 kPa : 0,6709.10-3 g.cm-3 | -182,47°C | -161,52°C | -82,6°C | 4 600 kPa | -182,47°C | 11,7 kPa | 537°C | entre 4,4 et 17 % en volume | à 25°C : 22,7 mg/L eau |
Voir le focus Gaz naturel.
Commentaires récents