Le magnésium est le huitième élément le plus abondant dans la croûte terrestre.
Il fait partie de la famille des métaux alcalino-terreux. Il s’agit d’un des métaux les plus légers, il est moins dense que le fer et même que l’aluminium. Sa forme la plus stable est l’ion Mg2+.
Son nom vient du nom de la ville Magnesia qui était connue pour les vertus de ses eaux salées dans l’Antiquité. Il faut cependant attendre 1808 pour que le l’électro-chimiste britannique, Humphry Davy, isole l’élément qu’il appellera Magnésium.
Données physico-chimiques
Données atomiques
| Numéro atomique |
Masse atomique |
Configuration électronique |
Structure cristalline |
Rayon métallique pour la coordinence 12 |
| 12 | 24,305 g.mol-1 | [Ne] 3s2 | Hexagonale compacte de paramètres a = 321 pm et c = 521 pm | 160 pm |
Données physiques
| Masse volumique | Dureté | Température de fusion | Température d’ébullition | Conductibilité électrique | Conductibilité thermique | Solubilité dans l’eau froide | Solubilité dans l’eau chaude |
| 1,74 g.cm-3 | 2,5 | 648,8°C | 1 090°C | 22,6.106 S.m-1 | 156 W.m-1.K-1 | insoluble | oxydé en Mg(OH)2 |
Données chimiques
| Électronégativité de Pauling | État d’oxydation | pKa : Mgaq2+/MgOHaq+ |
E° : Mg2+ + 2e = Mg(s) |
pKs : Mg(OH)2 | pKs : MgCO3 |
| 1,31 | +2 | 11,4 | -2,37 V | 11,0 | 7,5 |
Données thermodynamiques
Magnésium cristallisé
|
Magnésium gazeux
|
Données industrielles
Matières premières
La teneur en magnésium de l’écorce terrestre est d’environ 2 %. Il est abondant et bien réparti dans le monde en étant présent dans plus de 60 minéraux, dont les plus importants sont :
- la magnésite ou giobertite : MgCO3, voir le chapitre carbonate de magnésium.
- la dolomite qui renferme de la dolomie (Ca,Mg)CO3, avec une teneur de 38 % de MgO après calcination,
- la carnallite : KCl,MgCl2,6H2O, présente dans des gisements de potasse. Elle est utilisée, en particulier, comme source de magnésium dans les engrais,
- la bischofite : MgCl2,6H2O, voir le chapitre chlorure de magnésium.
- la kiesérite : MgSO4,H2O, utilisée dans l’industrie des engrais,
- la brucite : Mg(OH)2,
- l’olivine : silicate de magnésium et de fer avec une composition comprise entre celle de la forstérite (Mg2SiO4) et celle de la fayalite (Fe2SiO4). La qualité commercialisée comme source de magnésium renferme de 45 à 51 % de MgO et de 7 à 8 % de Fe2O3. Le principal producteur mondial est la Norvège.
Le magnésium est également récupéré dans l’eau de mer et dans des saumures, voir le chapitre chlorure de magnésium. La teneur de l’eau de mer est en moyenne de 1,3 kg/m3 soit 0,13 %. Certaines mers ou lacs fermés en contiennent jusqu’à 35 kg/m3. Par exemple, la teneur du Grand Lac Salé dans l’Utah, aux États-Unis, est, en masse, de 5 % en magnésium. Le magnésium est extrait sous forme de chlorure de magnésium MgCl2 et éventuellement transformé en oxyde MgO, en d’autres composés : hydroxyde, sulfate… ou en métal. Par exemple, aux États-Unis, en 2019, le magnésium extrait de l’eau de mer ou de saumures est à l’origine de 73 % de la production de sels de magnésium du pays. En 2017, dans le monde, la part provenant de l’eau de mer et des saumures est de 5,6 %. Toute la production primaire de magnésium métal des États-Unis et d’Israël provient du Grand Lac Salé pour l’un et de la Mer Morte pour l’autre.
Par exemple, en 2018, aux États-Unis, la production provient, exprimée en capacités annuelles de production d’équivalent en MgO :
- d’une carrière de magnésite à Gabbs, dans le Nevada par Premier Magnesia avec 140 000 t/an,
- d’une carrière d’olivine à Bellingham, dans l’État de Washington par Olivine Corp.,
- d’eau de mer à Chula Vista, en Californie par South Bay Salt Works avec 3 000 t/an,
- d’eau de mer à Lewes, dans le Delaware par SPI Pharma avec 5 000 t/an,
- de puits d’extraction de saumure à Manistee, dans le Michigan par Martin Marietta Magnesia Specialties avec 314 000 t/an,
- de lac salé à Ogden, dans l’Utah par Compass Minerals avec 290 000 t/an,
- de lac salé à Wendover, dans l’Utah par Intrepid Potash avec 45 000 t/an.
Métallurgie
Elle est réalisée actuellement selon 2 voies :
- Par réduction thermique de MgO issu de la calcination de dolomite ou de magnésite en présence de calcaire selon les procédés : Pidgeon, Bolzano ou Magnetherm. Le principal procédé utilisé est le procédé Pidgeon, employé pour la plus grande partie de la production chinoise.
- Par électrolyse, en sel fondu, de MgCl2 extrait de l’eau de mer, de saumures ou obtenu à partir de carnallite selon les procédés Dow, Norsk Hydro ou IG Farben.
- Par ailleurs, des projets sont en cours de développement, au Canada, dans la province de Québec, afin de traiter les résidus de l’exploitation de l’amiante, renfermant de la serpentine (3MgO,2SiO2,2H2O).
- Un projet développé par Latrobe Magnesium est également en cours de construction, en Australie, dans l’État de Victoria, afin de récupérer, avec un taux de récupération de 90 %, le magnésium contenu dans des cendres volantes issues de la centrale thermique de Yallourn produisant de l’électricité à partir de lignite. Le stock accumulé est considérable avec 25 millions de t renfermant jusqu’à 12 % de MgO contenu dans de la magnésioferrite, Mg(Fe3+)2O4 de structure spinelle, et la production annuelle de 320 000 t.
Réduction thermique par le silicium selon le procédé Pidgeon
Ce procédé mis au point en 1940, au Canadian National Research Council par Lloyd Montgomery Pidgeon a été industrialisé en 1942, à Haley, en Ontario, par la société Dominium Magnesium. L’usine a été fermée par la société Timminco Metals en 2008.
La dolomite (voir le produit carbonate de magnésium) ou la magnésite en présence de calcaire est d’abord décarbonatée dans un four rotatif entre 1000 et 1200°C. Ensuite, après broyage, ajout de ferrosilicium (à 78 % de Si) comme agent réducteur et de fluorure de calcium, pressage et briquetage, la matière première est introduite dans un four porté à 1200°C, sous vide (avec une pression d’environ 100 Pa). Le chauffage est effectué extérieurement (en Chine, le gaz de chauffage est souvent issu de cokeries). La réaction représentée selon l’équation suivante a lieu :
2 MgO,CaO + SiFe = 2 Mg(g) + Ca2SiO4 + Fe
Le magnésium, à l’état de vapeur, est condensé, dans une chambre refroidie par circulation extérieure d’eau. La réduction dure environ 6 h. Le magnésium obtenu possède une pureté élevée qui peut atteindre 99,95 %. Ce procédé présente l’inconvénient d’être discontinu, de faible productivité avec une production de 40 à 70 kg par four et de consommer une importante quantité d’énergie, avec environ 300 GJ/t. Toutefois, les investissements nécessaires sont réduits.
En Chine, les coût de production à l’aide du procédé Pidgeon se répartissent entre le ferrosilicium pour 48 %, l’énergie pour 15 %, la dolomite pour 6 %.
Électrolyse de MgCl2 selon le procédé Dow
C’est le procédé le plus ancien.
Mg2+ contenu dans des solutions de chlorure de magnésium provenant soit d’eau de mer, soit de saumures, est précipité, à l’aide de dolomie calcinée, en Mg(OH)2 qui est récupéré par filtration. L’hydroxyde est ensuite transformé en MgCl2,6H2O par attaque chlorhydrique, puis déshydraté partiellement en MgCl2,1,5H2O ou totalement pour alimenter les cuves d’électrolyse.
L’électrolyte qui fond vers 720-780 °C a la composition suivante :
| NaCl | CaCl2 | MgCl2 |
| 50-60 % | 15 % | 20-30 % |
Les anodes sont en graphite. Dans le cas des cellules Dow, les anodes sont entourées par des cathodes en acier percées de déflecteurs dont la forme permet de guider le magnésium formé vers le pourtour de la cellule, à l’abri de l’oxydation. Le magnésium, liquide, surnage sur le mélange de sels fondu. La consommation énergétique est de 12 000 kWh/t, pour les cellules les plus modernes.
L’un des problèmes lié à l’obtention du magnésium par électrolyse est l’utilisation l’hexafluorure de soufre SF6, servant à protéger le magnésium fondu de l’oxydation à l’air. L’hexafluorure de soufre est un gaz à effet de serre qui possède un potentiel de réchauffement global 22 800 fois plus important que le dioxyde de carbone (voir le chapitre effet de serre). Il est remplacé par du dodécafluoro-2-méthyl-3-pentanone ou par du dioxyde de soufre.
Projets québécois de traitement de la serpentine
Au Québec, l’exploitation de l’amiante sous forme de chrysotile (Mg3Si2O5(OH)4) de 1877 à 2011 a laissé des quantités considérables de rejets miniers, environ 800 millions de t, d’une roche, la serpentine, famille de minéraux à laquelle appartient le chrysotile, avec une teneur en magnésium d’environ 25 %. Diverses sociétés envisagent de produire du magnésium à partir de cette matière première située dans le sud-est de la province à Asbestos et à Thetford Mines.
- Alliance Magnésium (AMI) envisage un procédé hydrométallurgique de lixiviation à l’aide d’acide chlorhydrique avec formation de chlorure de magnésium suivi d’une électrolyse donnant le métal et une capacité de production de 11 700 t/an en 2022, pouvant être portée à 50 000 t/an.
- Mag One Products développe un procédé hydrométallurgique donnant de l’oxyde de magnésium avec une capacité de production de 30 000 t/an ainsi que de la fumée de silice et du magnésium par réduction de MgO par aluminothermie et une capacité de production de 5 000 t/an.
Projet australien de traitement de cendres volantes
Il associe un traitement hydrométallurgique donnant de l’oxyde MgO à un traitement pyrométallurgique de réduction à l’aide de ferrosilicium de type procédé Pidgeon. Le traitement hydrométallurgique consiste en une série de dissolutions dans de l’hydroxyde de sodium puis dans de l’acide chlorhydrique afin de dissoudre la magnésioferrite. Du carbonate de calcium et de l’hématite (Fe2O3) précipitent puis du chlorure de magnésium est récupéré et par calcination transformé en oxyde, le chlorure d’hydrogène formé étant recyclé pour donner de l’acide chlorhydrique. Cet oxyde, par pyrométallurgie, est réduit par du ferrosilicium en magnésium.
La production prévue pour 2021 est de 3 000 t/an et elle pourrait ensuite être portée à 40 000 t/an.
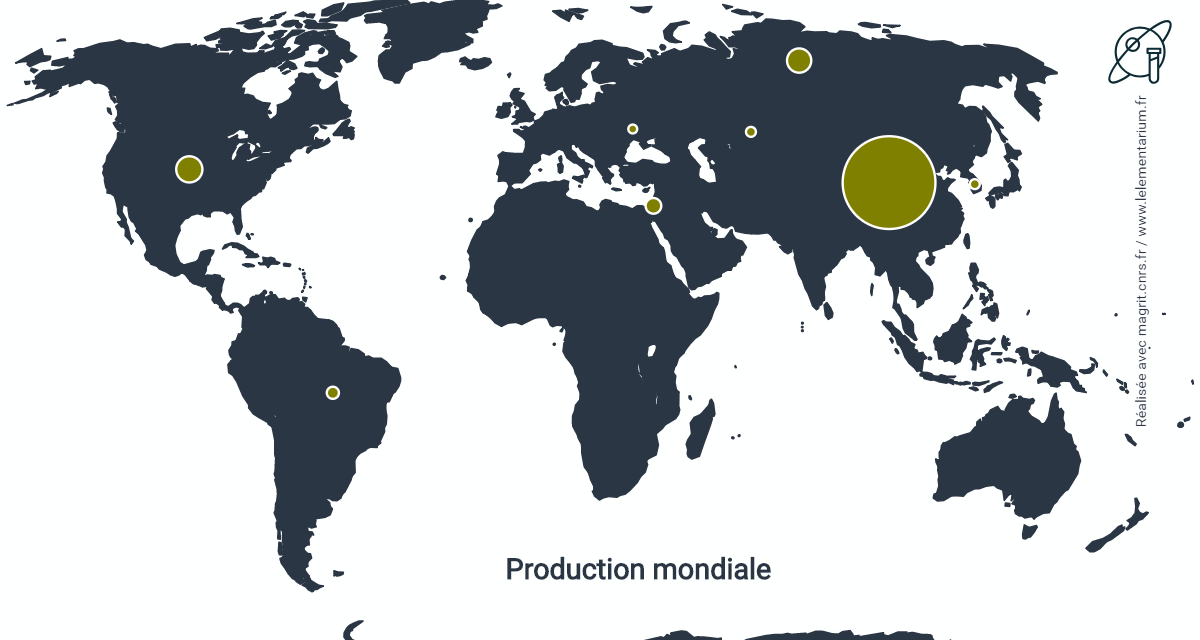
Production
En 2019, la production mondiale était de 1,1 million de t.
| Chine | 900 | Israël | 20 | |
| Russie | 80 | Brésil | 15 | |
| États-Unis (estimation) | 63 | Ukraine | 10 | |
| Kazakhstan | 25 | Turquie | 5 |
Sources : USGS et Solikamsk Magnesium Works
Il n’y a pas de production primaire dans l’Union européenne.
Fin 2018, la capacité mondiale de production de magnésium primaire est estimée à 1,855 million de t/an.
Il y a, en 2018, en Chine, plus de 60 usines utilisant le procédé Pindgeon, avec 58 % de la production provenant de la province du Shaanxi et 26 % de celle du Shanxi.
Commerce international : en 2019, y compris les déchets et les ouvrages en magnésium.
Principaux pays exportateurs :
| Chine | 455 554 | États-Unis | 11 769 | |
| Pays Bas | 74 148 | Slovénie | 10 651 | |
| Allemagne | 22 112 | Taipei chinois | 8 196 | |
| Canada | 14 823 | République tchèque | 7 477 | |
| Nouvelle Zélande | 12 103 | Turquie | 7 320 |
Source : ITC
Les exportations de la Chine sont destinées à 22 % aux Pays Bas, 13 % au Canada, 7 % au Japon…
Principaux pays importateurs sur un total de 708 190 t, en 2017.
| Pays Bas | 88 550 | Inde | 26 813 | |
| Canada | 75 459 | Corée du Sud | 23 492 | |
| Allemagne | 69 028 | Roumanie | 21 237 | |
| États-Unis | 62 958 | Taipei chinois | 17 547 | |
| Japon | 34 679 | Turquie | 17 465 |
Source : ITC
Les importations des Pays Bas proviennent à 94 % de Chine.
Principaux producteurs de magnésium, en 2018, hors celui auto-consommé pour produire l’éponge de titane, avec un total mondial de 935 000 t :
| Sociétés chinoises | 800 |
Rima Industrial (Brésil) | 15 | |
| US Magnesium (États-Unis) | 63 | VSMPO-Avisma (Russie) | 7 | |
| Dead Sea Magnesium (Israël) | 25 | Royal Metal (Iran) | 5 | |
| Solikamsk Magnesium Works (Russie) | 16 | Esan (Turquie) | 3 |
Source : Solikamsk Magnesium Works
- Rare Earth Magnesium Technololy Group filiale du groupe Century Sunshine Group Holdings Ltd. exploite une mine à ciel ouvert de dolomite à Baishan dans la province de Jilin et produit du magnésium à Hami dans la région autonome ouïghoure du Xinjiang avec, en 2019, 60 559 t d’alliages de magnésium.
- La société QingHai Salt Lake exploite le chlorure de magnésium contenu dans le lac salé de Qarham, à 2800 m d’altitude sur le plateau tibétain, dans la province de Qinghai et produit, à Golmud, par électrolyse, du magnésium. Celui-ci approvisionne l’usine d’élaboration d’alliages de magnésium de la société australienne Magontec. La production, par électrolyse, selon le procédé Norsk Hydro, a débuté en octobre 2018 avec une capacité de production de 56 000 t/an. Le dichlore coproduit lors de l’électrolyse est destiné à la production de PVC. Toutefois les difficultés de fonctionnement de Qinghai Salt Lake n’ont pas permis un approvisionnement suffisant et, en 2019, la production de magnésium n’a été que de 9 267 t.
- Yinguang Magnesium Industry possède, à Yaocun, dans la province du Shanxi, une capacité de production de 80 000 t/an.
- US Magnesium LLC (Utah, États Unis) est le seul producteur aux États Unis, à Rowley, dans l’Utah, avec une usine exploitant les saumures du Grand Lac Salé et produisant du magnésium par électrolyse avec une capacité de production de 63 500 t/an.
- Dead Sea Magnesium, filiale de Israel Chemicals Ltd. (Israël), avec une capacité de production de 24 000 t/an, exploite, à Sodom, l’eau de la Mer Morte. En 2019, la production a été de 21 000 t. La solution de chlorure de magnésium obtenue à partir de la carnallite extraite de la Mer Morte est électrolysée pour donner du magnésium et du dichlore employé dans la production de dibrome (voir ce chapitre).
- En Russie, les sociétés productrices Solikamsk Magnesium Works et VSMPO-Avisma sont aussi productrices de titane. En conséquence, une partie de leur production est auto-consommée par cette application. Solikamsk Magnesium Works possède une capacité de production de 18 200 t/an par électrolyse et a vendu, en 2018, 16 200 t de magnésium à partir de carnallite et VSMPO-Avisma a vendu, 7 000 t.
- Rima (Brésil) à Bocaiuva, dans l’État du Minas Gerais possède une capacité de production de 22 000 t/an à partir d’une production minière de 180 000 t/an de dolomite.
- Kar Magnesium Smelter produit du magnésium en Turquie depuis 2016, avec une capacité de production de 15 000 t/an, à Emirdag, dans la province d’Afyonkarahisar, à l’aide du procédé Pidgeon, à partir de dolomite. En 2019, la production est de 4 500 t.
- « UKTMK » (Ust-Kamenogorsk Titanium-Magnesium Combine) (Kazakhstan) possède une capacité de production de 30 000 t/an et auto-consomme la plus grande partie de sa production pour la fabrication d’éponge de titane.
- Zaporozhye Titanium & Magnesium Combine (Ukraine) possède une capacité de production de 15 000 t/an par électrolyse en sel fondu de chlorure de magnésium et de carnallite. La quasi totalité de la production est employée à fabrication d’éponge de titane.
- Mg Serbien (Serbie) produit 5 000 t/an à Baljevac, selon le procédé Magnetherm à partir de dolomite.
Recyclage
La production mondiale de magnésium secondaire est estimée à 200 000 t/an, hors recyclage du magnésium contenu dans les alliages d’aluminium directement recyclés. La production de magnésium de deuxième fusion est, en 2019, de 110 000 t aux États Unis, dont 85 000 t provenant de chutes neuves et 25 000 t de métal récupéré, les alliages d’aluminium comptant pour 67 % de l’approvisionnement. Toutefois, aux États-Unis, le chlorure de magnésium sous-produit de la métallurgie du titane et recyclé avec la production de magnésium primaire n’est pas prise en compte.
En 2012, dans l’Union européenne, le recyclage a porté sur 63 300 t dont 51 700 t de chutes neuves de fabrication et 11 700 t de vieux déchets.
Situation française
En 2019.
La production de magnésium qui était réalisée par Pechiney Électrométallurgie à Marignac (31), selon le procédé Magnetherm, à partir de dolomite, avec 12 500 t/an, a cessé en juillet 2001.
Commerce extérieur :
Les exportations étaient confidentielles.
Les importations s’élevaient à 12 268 t en provenance principalement à :
- 47 % de Chine,
- 35 % d’Allemagne,
- 7 % d’Israël.
Utilisations
Consommations
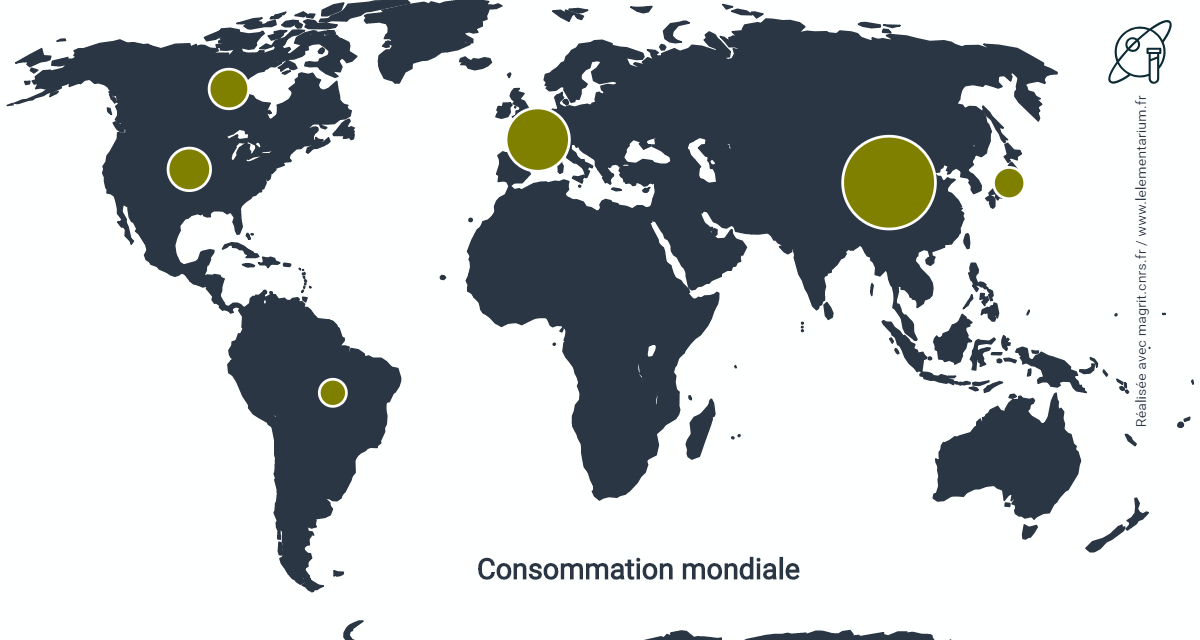
En 2016, la consommation mondiale de magnésium primaire est de 843 000 t répartie entre les pays suivants :
| Chine | 352 | Canada, en 2014 | 64 | |
| Union européenne, en 2014 | 164 | Japon | 40 | |
| États-Unis | 74 | Brésil, en 2014 | 30 |
Sources : Solikamsk Magnesium Works, USGS et A. Clark, World Magnesium Conference Technical, 2017
Secteurs d’utilisation
Les secteurs utilisateurs sont principalement :
| Monde, en 2016 |
Chine, en 2016 |
États-Unis, en 2019 |
|||
| Alliages de Al | 37 % | 33 % | 28 % | ||
| Alliages de Mg | 32 % | 30 % | 55 % | ||
| Désulfuration de l’acier | 15 % | 13 % | 13 % | ||
| Agent de réduction (Ti) | 10 % | 17 % | – |
Sources : USGS, Solikamsk Magnesium Works et A. Clark, World Magnesium Conference Technical, 2017
- Alliages d’aluminium : le magnésium entre dans la composition des alliages (série 5000) utilisés pour élaborer les boîtes-boisson. Aux États-Unis, une grande partie du magnésium utilisé est recyclé lors du recyclage de ces boîtes. En moyenne, les alliages d’aluminium renferment 0,8 % de magnésium, soit, en 2015, une consommation de 350 000 t de magnésium.
- Alliages de magnésium : utilisés en fonderie sous pression, à 70 % dans l’industrie automobile. Le plus utilisé G-A9Z1 (9 % Al, 1 % Zn, 0,5 % Mn). En moyenne, par véhicule il y a 2,3 kg de magnésium mais le poids peut atteindre 23 kg pour certains modèles. Utilisés également en aéronautique et, par exemple, pour fabriquer le corps de taille-crayons. Un cadre de bicyclette, en alliage de magnésium, ne pèse que 2,5 kg. En 2015, l’élaboration des alliages de magnésium a consommé 315 000 t.
- Le magnésium est employé comme agent de réduction (par magnésiothermie) dans diverses métallurgie dont principalement celle du titane, mais aussi celles du zirconium, du hafnium, du béryllium, de l’uranium (voir ces éléments). En 2015, la production de l’éponge de titane a consommé 130 000 t de magnésium mais une partie de celui-ci est recyclé par électrolyse du chlorure de magnésium formé selon le procédé Kroll et en conséquence, la consommation de magnésium primaire a été proche de 80 000 t.
- En sidérurgie, le magnésium intervient dans la désulfuration des fontes de hauts fourneaux, en concurrence avec le carbure de calcium et dans la nodulisation des fontes, le magnésium favorisant les structures à graphite nodulaire sphéroïdal. En moyenne, la consommation est de 50 g de Mg/t d’acier, soit, en 2015, une consommation de 95 000 t.
Utilisations diverses
Quelques autres exemples d’utilisations :
- Chimie : fabrication d’organomagnésiens.
- Automobiles : le magnésium est utilisé afin de réduire le poids des véhicules et ainsi diminuer leur consommation en carburant. Il y a 14 kg de magnésium utilisé pour les VW Passat, Audi A4 et A6. Le concept car de Volvo utilise environ 50 kg de magnésium dans les roues, les châssis et les moteurs.
- Les coques des sièges, les accoudoirs et les tablettes des TGV à 2 étages sont, en 2ème classe, en magnésium. Le siège en magnésium pèse 14 kg au lieu de 26 kg lorsqu’il était en aluminium.
- Le magnésium est utilisé pour fabriquer des cadres de téléphones portables.
- Débismuthage du plomb.
- Pyrotechnie : Mg ou Al-Mg sous forme de poudres très fines.
- Piles et anodes sacrificielles : l’utilisation comme anode sacrificielle représente 1 010 t, en 2014, aux États-Unis.
- Les rubans de magnésium utilisés en chimie sont obtenus par fraisage de lingots ou tournage de billettes (cylindres de 30 à 50 cm de diamètre et plusieurs mètres de long).
- La réaction exothermique du magnésium avec l’eau est utilisée, en particulier par l’armée américaine, pour chauffer des rations de combat. En 15 minutes, une température de 60 °C est atteinte.
Bibliographie
- Morgo Magnesium Limited, PO Box 342, 7200 AH Zutphen, Pays-Bas.
- International Magnesium Association, 1000 N Rand rd, Suite 214, Wauconda, IL 60084, États-Unis.
- MMTA, Suite 53, 3 Whitehall Court, Londres, SW1A 2EL, Royaume Uni.
- Life cycle assessment of magnesium components in vehicle construction, IMA LCA Study, DLR, mai 2013.
- N. Bell, R. Waugh, D. Parker, « Magnesium recycling in the EU« , IMA juin 2017.
- P. Blazy et V. Hermant, Techniques de l’Ingénieur, 2013.
- D.C. Lynch, « Magnesium Minerals and Metal », in SME Mineral Processing & Extraction Metallurgy Handbook, chapter 12.21, p1855, Society for Mining, Metallurgy & Exploration, 2019.