L’attribution de la découverte du vanadium reste en débat. En effet, il semblerait qu’il ait été découvert il y a plus de 200 ans par le baron allemand A. von Humbolt. Cependant, ses échantillons et ses notes ayant sombré lors du naufrage de son bateau, aucune preuve ne subsiste . Il faudra attendre 1831 et le suédois Nils Selfström pour avoir des preuves de l’existence de ce métal. On lui doit également son nom, de Vanadis qui est la déesse scandinave de la beauté et de la fertilité.
Données physico-chimiques
Données atomiques
| Numéro atomique | Masse atomique | Configuration électronique | Structure cristalline | Rayon métallique pour la coordinence 12 |
| 23 | 50,94 g.mol-1 | [Ar] 3d3 4s2 | cubique centrée de paramètre a = 0,302 nm | 134,6 pm |
Données physiques
| Masse volumique | Dureté | Température de fusion | Température d’ébullition | Conductibilité électrique | Conductibilité thermique | Solubilité dans l’eau |
| 5,96 g.cm-3 | 6,7 | 1 890°C | 3 380°C | 4,89.106 S.m-1 | 30,7 W.m-1.K-1 | insoluble |
Données chimiques
| Électronégativité de Pauling | pKs : VO2(OH) | |
| 1,63 | 14,7 |
pKa :
| V3+aq/VOH2+aq | pKa = 2,9 |
| VOH2+aq/V(OH)2+aq | pKa = 3,5 |
| VO2+aq/VOOH+aq | pKa = 5,4 |
| VO3–/HVO42- | pKa = 8 |
Potentiels standards :
| VO2+ + 2H+ + e = VO2+ + H2O | E° = 0,999 V |
| VO2+ + 4H+ + 5e = V(s) + 2H2O | E° = -0,25 V |
| HV6O173- + 16H2O + 30e = 6V(s) + 33OH– | E° = -1,15 V |
| VO2+ + 2H+ + e = V3+ + H2O | E° = 0,34 V |
| V3+ + e = V2+ | E° = 0,255 V |
| V2+ + 2e = V(s) | E° = -1,2 V |
Données thermodynamiques
Vanadium cristallisé
|
Vanadium gazeux
|
Données industrielles
Matières premières
La teneur en vanadium (V) de l’écorce terrestre est de 0,016 %.
Le vanadium, est le plus souvent récupéré à partir de titanomagnétites vanadifères qui peuvent renfermer jusqu’à 3 % de V2O5. Dans les titanomagnétites, le titane se substitue au fer de la magnétite pour donner un oxyde mixte de formule Fe3-xTixO4.
Par exemple :
- le gisement Windamurra, en Australie, renferme 55 % de Fe, 14 % de TiO2 et 0,47 % de V2O5 ;
- celui de Mapochs, en Afrique du Sud, 1,4 % de V2O5.
Lorsque la teneur en oxyde de vanadium est supérieure à 1-1,5 %, le minerai peut être traité directement pour le récupérer, cela est le cas en Afrique du Sud et en Chine et donne, en 2018, 18 % de la production mondiale de vanadium. Pour des teneurs inférieures, l’oxyde de vanadium est extrait du laitier obtenu lors de l’utilisation des minerais de titanomagnétite vanadifère pour élaborer de l’acier, cela est le cas, en Chine, en Nouvelle Zélande et en Russie dans 9 aciéries qui possèdent une capacité de production d’acier de 33 millions de t/an et donnent, en 2018, 70 % de la production mondiale de vanadium.
La concentration des minerais renfermant des titanomagnétites vanadifères est facilitée par leurs propriétés magnétiques.
Du vanadium est également présent dans du charbon, du pétrole, des sables bitumineux et est récupéré dans les cendres après combustion du charbon ou dans les résidus pétroliers, lors de son raffinage. Il est également récupéré lors du recyclage de catalyseurs. On estime que cette source représente, en 2018, 12 % de la production mondiale de vanadium.
Du vanadium est aussi présent dans des minerais d’uranium (carnotite) extraits aux États-Unis qui contiennent de 1 à 5 % de V2O5, des minerais d’alumine (roscoelite) extraits en Inde, des sables riches en oxyde de fer (80 % de Fe3O4, 8 % de TiO2, 0,6 % de V2O5), en Nouvelle Zélande. Par exemple, la société Energy Fuels a extrait, en 2013, 594 t de V2O5 et 459 t de U3O8 lors du traitement de minerais d’uranium dans l’usine de White Mesa, dans l’Utah, aux États-Unis. En 2014, cette coproduction a été suspendue.
Élaboration industrielle
Les titanomagnétites riches en vanadium, par exemple en Afrique du Sud, sont calcinées, en présence de carbonate, chlorure ou sulfate de sodium, dans un four, à 850°C. Il se forme du vanadate de sodium (NaVO3) qui est extrait par lixiviation à l’eau, puis l’ajout d’ammoniac permet la précipitation du vanadate d’ammonium. La calcination de ce dernier dans des conditions déterminées donne l’oxyde désiré.
Les titanomagnétites plus pauvres en vanadium sont principalement traitées dans un haut fourneau puis un convertisseur, en Chine ou en Russie.
Le traitement dans un haut fourneau donne d’une part un laitier riche en dioxyde de titane d’où ce dernier sera extrait (voir le chapitre dioxyde de titane) et d’autre part de la fonte contenant le vanadium. Ce dernier sera récupéré sous forme de V2O5 dans un convertisseur, lors de l’élaboration de l’acier à partir de la fonte et du soufflage du dioxygène destiné à diminuer la teneur en carbone.
En Afrique du Sud, le minerai qui était extrait par Evraz de la mine de Mapochs subissait un traitement en 3 étapes de pré-réduction puis de réduction dans un four électrique et enfin d’oxydation. Il était pré-réduit, en présence de charbon en poudre, dans un four tournant vers 1 140°C puis, réduit, vers 1 350°C dans un four électrique à électrode immergée dans lequel à lieu la séparation entre un laitier riche en dioxyde de titane et une fonte contenant le vanadium, avec une teneur de 1,28 % de V. Celle-ci subissait ensuite, dans une poche de coulée, un soufflage de dioxygène qui permet de recueillir dans un nouveau laitier, le vanadium sous forme d’oxyde, avec une teneur comprise entre 12 et 16 % de V. Les sables riches en magnétite de Nouvelle Zélande, exploités par New Zealand Steel, subissent un traitement proche.
Les laitiers obtenus comme coproduits des opérations sidérurgiques sont ensuite traités comme les minerais riches en vanadium.
Le vanadium contenu dans les pétroles lourds se retrouve, dans le coke produit lors du procédé flexicoke de transformation des pétroles lourds en produits plus légers. Le vanadium renfermé dans le coke est extrait par de l’acide sulfurique puis précipité par de l’ammoniac, en vanadate d’ammonium. Le principe d’extraction est le même pour le vanadium contenu dans les cendres des centrales thermiques fonctionnant au charbon.
Les oxydes de vanadium sont principalement utilisés pour produire, par aluminothermie ou par réduction au four électrique du ferrovanadium destiné à la fabrication d’acier ou des alliages vanadium-aluminium destinés à la métallurgie du titane.
Le vanadate d’ammonium ou les oxydes purifiés sont à la base de l’élaboration des divers composés chimiques du vanadium.
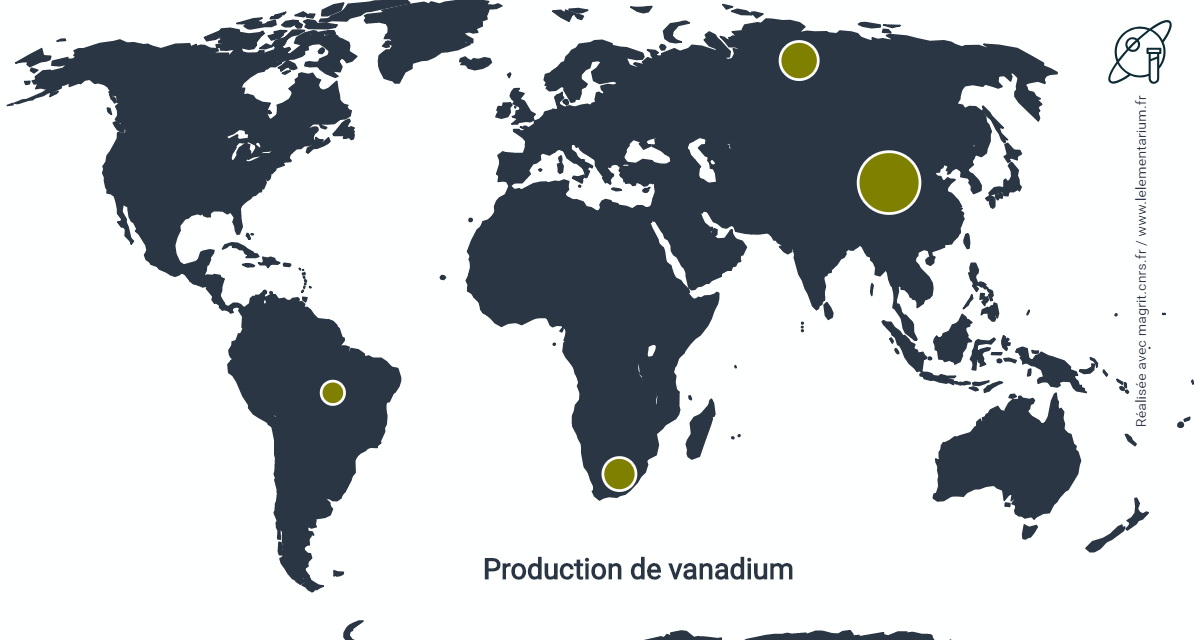
Productions
En 2019, la production mondiale était de 73 000 t de vanadium contenu en provenance des pays suivants :
| Chine | 40 000 t | Afrique du Sud | 8 000 t | |
| Russie | 18 000 t | Brésil | 7 000 t |
Source : USGS
Au Brésil, a débuté, en août 2014, la production de la mine de Maracás Menchen, dans l’État de Bahia, exploitée par la société canadienne Largo Resources. En 2019, la production est de 10 577 t de V2O5 destinée par contrat jusqu’en mai 2020 au groupe Glencore. En 2019, 1,156 million de t de minerai ont été extraites avec une teneur de 1,34 % de V2O5. La production de concentrés a été de 382 501 t avec une teneur de 3,29 % de V2O5, et un taux de récupération de 78,5 %. Les réserves prévues et probables sont de 19 millions de t de minerai renfermant 1,15 % de V2O5.
La mine de Windimurra, en Australie, propriété d’Atlantic, qui avait commencé à produire a dû cesser toute production après un incendie qui a détruit l’usine d’enrichissement le 4 février 2014. Les réserves prouvées et probables sont, en mars 2015, de 55,1 millions de t contenant 0,49 % de V2O5. La mine, à ciel ouvert, est située en Australie Occidentale, à 660 km au nord de Perth. Le minerai contient outre le vanadium, 55 % de fer et 14 % de TiO2. La capacité de production prévue est de 7 750 t de V2O5, en 2020.
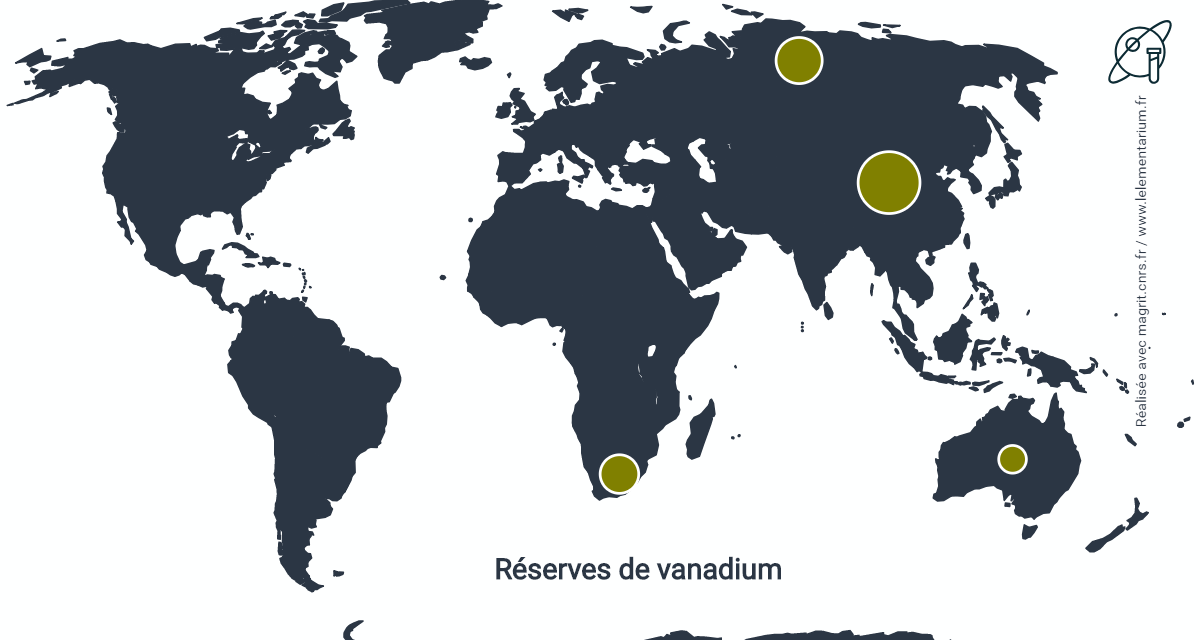
Réserves minières
En 2019, les réserves mondiales sont estimées à 22 millions de t, réparties dans les pays suivants :
| Chine | 9 500 | Australie | 4 000 | |
| Russie | 5 000 | Afrique du Sud | 3 500 |
Source : USGS
En Chine, 83,2 % des réserves chinoises de titanomagnétites vanadifères sont situées dans la province du Sichuan.
Principaux producteurs
Les principaux producteurs de Vanadium sont :
- Des groupes chinois :
- Pangang Group Vanadium Titanium & Resources, n°1 mondial, avec 17 % de la production mondiale, dans la province du Sichuan, avec une capacité de production de 260 000 t/an de laitiers, 22 000 t/an de V2O5, 16 000 t/an de ferrovanadium.
- Chengde XinXin Vanadium & Titanium, dans la province de Hebei.
- China Vanadium Titano-Magnetite Mining Company, exploite dans la province du Sichuan, en Chine, 2 mines actives : Baicao et Xiushuihe. En 2018, la production de concentrés, avec une teneur en fer de 54 %, a été de 1,111 million de t. Les réserves prouvées et probables, fin 2018, de la mine de Baicao sont de 9,13 millions de t de minerai contenant 20,76 % de Fe, 10,70 % de TiO2 et 0,23 % de V2O5. Celles de la mine de Xiushuihe sont de 45,64 millions de t contenant 24,11 % de Fe, 9,04 % de TiO2 et 0,21 % de V2O5.
- Evraz, groupe russe, est n°2 mondial, avec 13 % de la production mondiale, en produisant de l’oxyde de vanadium et du ferrovanadium, en Russie, en République tchèque et aux États-Unis. En 2018, la production de vanadium contenu dans des laitiers, réalisée exclusivement en Russie, a été de 17 052 t. En 2018, Les ventes ont été de 6 842 t de vanadium contenu dans des laitiers et 12 352 t de vanadium renfermé dans des alliages et des produits chimiques.
- En Russie, Evraz exploite, à Kachkanarsky, avec 3 mines à ciel ouvert, le dépôt de titanomagnétite vanadifère de Gusevogorskoye, qui possède des réserves de 3,108 milliards de t de minerai contenant 15,9 % de fer, 5 % de TiO2 et 0,13 % de V2O5, les laitiers sont produits par les installations sidérurgiques de Nizhny Tagil, dans la région de Sverdlovsk, et transformés, en ferrovanadium et oxyde de vanadium, à Tula, avec une capacité de production de 7 500 t/an d’oxyde de vanadium et 5 000 t/an de ferrovanadium.
Par ailleurs, le gisement de Kachkanar Proper possède 6,743 milliards de t de réserves prouvées et probables renfermant 16,5 % de fer et 0,14 % de V2O5. - En République tchèque, à Mnisek pod Brdy, Evraz a une capacité de production de 4 600 t/an de ferrovanadium à partir d’oxyde produit à Tula.
- Aux États-Unis, la production d’oxyde de haute pureté et de divers composés chimiques du vanadium est effectuée à Hot Springs, dans l’Arizona, par Stratco filiale à 78,76 %, avec une capacité de production de 5 400 t/an d’oxyde de vanadium. En octobre 2019, cette activité a été vendue à la société US Vanadium Holding.
- En Afrique du Sud, Evraz exploitait, à 65 %, la mine de Mapochs, à Roossenekul dans la province de Limpopo, et produisait des laitiers à Emalahleni dans la province de Mpumalanga mais ces productions ont cessé après la faillite de la filiale l’Evraz, Evraz Highveld Steel and Vanadium. Par ailleurs, sa filiale Vametco a été vendue.
- En Russie, Evraz exploite, à Kachkanarsky, avec 3 mines à ciel ouvert, le dépôt de titanomagnétite vanadifère de Gusevogorskoye, qui possède des réserves de 3,108 milliards de t de minerai contenant 15,9 % de fer, 5 % de TiO2 et 0,13 % de V2O5, les laitiers sont produits par les installations sidérurgiques de Nizhny Tagil, dans la région de Sverdlovsk, et transformés, en ferrovanadium et oxyde de vanadium, à Tula, avec une capacité de production de 7 500 t/an d’oxyde de vanadium et 5 000 t/an de ferrovanadium.
- Glencore, exploite à 74 %, en Afrique du Sud, dans le complexe du Bushveld, la mine de Rhovan et a produit, à Brits, en 2019, 9 163 t de V2O5 sous forme d’oxyde et de ferrovanadium. Les réserves prouvées et probables étaient, fin 2019, de 32,6 millions de t renfermant 0,50 % de V2O5.
- Bushveld Minerals, a acquis, en 2016, Vametco, filiale de Evraz, en Afrique du Sud, qui produit des oxydes de vanadium et du vanadium nitré, à Brits dans la province du Nord-Ouest, avec, en 2019, une production de 2 833 t de vanadium. Les réserves prouvées et probables sont de 48,43 millions de t de minerai renfermant 28,5 % de magnétite et 2,02 % de V2O5 dans la magnétite. Par ailleurs, a acquis, en novembre 2019, la société Vanchem qui produit du ferrovanadium et des composés chimiques du vanadium à Highveld, en Afrique du Sud, avec, en 2020, une production prévue d’environ 1 000 t.
Commerce international
Il a porté, en 2011, sur 41 028 t de ferrovanadium et 31 219 t d’oxyde.
En 2013, les exportations de la Chine ont été de 6 074 t, celles de la Russie, de 1 416 t.
En 2019, en vanadium contenu, les importations des États-Unis ont été de 4 000 t de V2O5, 2 500 t de ferrovanadium, 140 t d’autres oxydes et hydroxyde, 240 t d’alliage Al-V, 60 t de métal, 2 100 t de cendres et déchets.
Recyclage
Le vanadium contenu, sous faible teneur, dans les aciers n’est pas récupéré.
Par contre celui contenu dans les aciers rapides et les superalliages est récupéré et recyclé. Il en est de même pour l’oxyde de vanadium des catalyseurs usés. La récupération des catalyseurs usés permet le recyclage de 3 000 t/an de vanadium.
Le recyclage représentait, en 2013, 11 % de la consommation.
Situation française
Il n’y a pas de production française.
Commerce extérieur
Exportations
Les exportations en 2019 étaient de :
- 51 kg pour les oxydes et hydroxydes vers principalement :
- à 65 % l’Espagne,
- 20 % le Maroc,
- 12 % le Portugal,
- 2 % la Roumanie.
- 69 t pour le ferrovanadium vers principalement:
- à 28 % l’Allemagne,
- à 17 % la Russie,
- à 13 % l’Italie,
- à 13 % le Canada,
- à 12 % la Turquie.
- 12 t pour le métal brut vers :
- à 100 % l’Afrique du Sud.
Importations
Les importations en 2019 étaient de :
- 464 t pour les oxyde et hydroxyde, en provenance principalement :
- à 43 % de Chine,
- à 26 % du Brésil,
- à 19 % de Taipei chinois.
- 714 t de ferrovanadium en provenance principalement :
- à 30 % des Pays Bas,
- à 23 % de République tchèque,
- à 16 % d’Autriche.
- 81 t de métal brut en provenance :
- à 60 % d’Allemagne,
- à 12 % des États-Unis,
- à 12 % d’Afrique du Sud.
Utilisations
Consommations
La consommation mondiale, en 2018, s’élevait à 94 975 t. Sa répartition, en 2016, était la suivante :
| Chine | 44 % | Japon | 6 % | |
| Europe | 18 % | Russie et CIS | 6 % |
|
| Amérique du Nord | 12 % | Inde | 4 % |
Source : VanadiumCorp
Secteurs d’utilisation
Les principaux secteur utilisateurs dans le monde, en 2017, étaient les suivants :
| Aciers | 91 % | Chimie | 3,5 % | |
| Alliages de titane et d’aluminium | 4,5 % | Autres (batteries…) | 1 % |
Le vanadium est introduit dans les aciers principalement, à 85 %, sous forme de ferrovanadium. Celui-ci renferme 40, 60 ou 80 % de vanadium. Ceux contenant 60 et 80 % de vanadium sont élaborés par aluminothermie ou réduction dans un four électrique. Ceux à 40 % de vanadium sont préparés par réduction à l’aide de silicium.
En moyenne, en 2018, dans le monde, la teneur des aciers en vanadium est de 0,054 kg de V/t d’acier, avec :
- 0,099 kg/t en Amérique du Nord,
- 0,077 kg/t en Europe,
- 0,053 kg/t au Japon,
- 0,048 kg/t en Chine,
- 0,012 kg/t en Inde.
Le vanadium, en formant des carbures et des nitrures, sous faible teneur, d’environ 0,25 %, comme le niobium ou le titane, permet d’obtenir des aciers micro-alliés, à haute résistance (aciers HSLA) qui représentent 12 % de la production mondiale d’aciers. Le rôle du vanadium est d’augmenter la limite élastique et la résistance à la traction, propriétés importantes pour les aciers destinés à la construction et en particulier les ronds à béton. Cette application dans les aciers HSLA représente, en 2014, 46 % des utilisations du vanadium.
Les aciers rapides ont des teneurs en vanadium comprises entre 1 et 5 %.
Le vanadium entre dans la composition du principal alliage de titane, TA6V, contenant 90 % de Ti, 6 % de Al et 4 % de V, utilisé dans l’aéronautique ainsi que pour des implants dentaires.
L’oxyde de vanadium, V2O5, est utilisé comme catalyseur dans le procédé de contact de fabrication de l’acide sulfurique. Il catalyse la réaction d’oxydation du dioxyde de soufre, en trioxyde. Il catalyse également la formation d’anhydride maléique, par oxydation à l’air du butane.
Le vanadium est utilisé dans des batteries stationnaires. Ces batteries redox au vanadium qui possèdent une capacité importante peuvent répondre à des pics de consommation ou au lissage de la production de sources intermittentes telles que le photovoltaïque ou l’éolien. La possibilité pour le vanadium de présenter, en solution, 4 différents degrés d’oxydation (+V, +IV, +III, +II) est mise à profit. La demi-cellule positive contient, en solution dans l’acide sulfurique, des ions VO2+ qui lors de la charge donnent des ions VO2+, la demi-cellule négative renfermant des ions V3+ donnant des ions V2+, le séparateur des cellules est une membrane perméable aux protons. La tension entre les 2 demi-cellules est de 1,41 V à 25°C.
Il est également utilisé dans des batteries au lithium. La technologie lithium-ions utilise des cathodes en oxyde de lithium-cobalt, LiCoO2 qui peuvent être remplacées par des cathodes en phosphate de lithium-vanadium, Li3V2(PO4)3, associé ou non à du phosphate de lithium-fer, LiFePO4. Ces batteries sont destinées à alimenter les véhicules électriques. Une technologie concurrente lithium-métal-polymère, utilise des cathodes en oxyde de vanadium, carbone et polymère. Cette technologie était utilisées par le groupe Bolloré pour alimenter les véhicules Blue Car d’Autolib, à Paris. Elle présente l’avantage de ne comporter que des composants solides évitant les risques d’explosion mais doit fonctionner à 85°C pour atteindre un fonctionnement optimal.
Utilisations diverses :
Colore en jaune les céramiques et les verres.
Bibliographie
- Vanitec, Winter House, High Street, Westerham, Kent, TN16 1AQ, Royaume Uni.
- « Le vanadium – éléments de criticité« , BRGM, décembre 2018.
- T. Perles, « Vanadium market fundamentals and implications« , Metal Bulletin 28th international ferroalloys conference, 13 nov. 2012, Berlin.
- P.R. Taylor, S.A. Shuey, E.E. Vidal, J.C. Gomez, Extractive Metallurgy of Vanadium-Containing Titaniferous Magnetite Ores: a Review, Society for Mining, Metallurgy, and Exploration, Inc. Mai 2006.
- J. Hykawy, Vanadium : the supercharger, Byron, novembre 2009.
- Report on resources for the steel industry prepared by ESTEP’s WG4, septembre 2012.
- T. G. Goonan, Vanadium Recycling in the United States in 2004, U.S. Geological Survey Circular 1196–S, Octobre, 2011.