Données physico-chimiques
Données atomiques
| Formule | Masse molaire |
| NaClO3 | 106,44 g.mol-1 |
Données physiques
| Masse volumique | Température de fusion | Température d’ébullition | Solubilité dans l’eau |
| 2,49 g.cm-3 | 248-261°C | décomposé |
|
Données chimiques
| pKa : HClO3/ClO3– | pKa : HClO2/ClO2– |
| -2,7 | 1,95 |
Potentiels standards :
| ClO4– + 2H+ + 2e = ClO3– + H2O | E° = 1,19 V |
| ClO4– + H2O + 2e = ClO3– + 2OH– | E° = 0,36 V |
| ClO3– + 2H+ + e = ClO2(g) + H2O | E° = 1,15 V |
| ClO3– + 3H+ + 2e = HClO2 + H2O | E° = 1,21 V |
| ClO3– + H2O + 2e = ClO2– + 2OH– | E° = 0,33 V |
| ClO3– + 6H+ + 5e = 1/2Cl2(g) + 3H2O | E° = 1,47 V |
| ClO2(g) + H+ + e = HClO2 | E° = 1,27 V |
| ClO2(g) + e = ClO2– | E° = 0,95 V |
Données thermodynamiques
Chlorate de sodium cristallisé :
- Enthalpie molaire standard de formation à 298,15 K : -358,8 kJ.mol-1
- Enthalpie molaire standard de fusion à la température de fusion : 22,6 kJ.mol-1
Données industrielles
Fabrication industrielle
La formation d’ions chlorate ClO3– (dans lesquels le chlore possède un nombre d’oxydation de +5) peut être réalisée par :
- Dismutation des ions hypochlorite ClO– (de nombre d’oxydation de +1) en phase homogène, vers 60-80°C et à pH compris entre 6,0 et 6,5, selon la réaction représentée par l’équation chimique suivante :
3 ClO– = 2 Cl– + ClO3–
- Oxydation électrochimique des ions hypochlorite ClO–.
Dans tous les cas, on part d’hypochlorite de sodium formé par électrolyse, dans des cellules sans séparateur, d’une solution saturée de chlorure de sodium NaCl. La réaction globale est la suivante :
Cl– + 3 H2O = ClO3– + 3 H2
Actuellement, de plus en plus, la formation des ions ClO3– est effectuée par dismutation des ions ClO–, dans un réacteur couplé à la cellule d’électrolyse de NaCl. Les cathodes sont en acier, les anodes de type DSA, la distance séparant les électrodes est de 3 à 5 mm. Un ajout de dichromate de sodium (1 à 5 g/L) permet d’éviter une réduction partielle de ClO– et ClO3–. La tension est de 2,75 à 3,60 V, les densités de courant de 15 à 25 A/dm2. La consommation électrique est de 5 000 à 6 000 kWh/t de chlorate de sodium (en 2017, pour une production mondiale de 3,6 millions de t, la consommation électrique est de 20 TWh). L’électrolyte circule rapidement (1 m/s) dans la cellule jusqu’à ce que la concentration en chlorate atteigne 625 g/L. Le pH est maintenu par ajout de HCl. Avant électrolyse, la saumure est purifiée afin d’éliminer, par précipitation et filtration, les ions calcium, magnésium, sulfate…, à l’aide d’hydroxyde de sodium, carbonate de sodium, chlorure de calcium ou de baryum, ces derniers pour éliminer les ions sulfate.
NaClO3 cristallisé, à 99,5 % de pureté, est obtenu par évaporation de l’eau, sous vide, puis séchage, généralement en lit fluidisé, par de l’air, à 150°C.
Co-production : du dihydrogène, avec 60 kg/t de chlorate de sodium.
Consommations : pour 1 t de NaClO3.
| NaCl | HCl à 100 % | NaOH | Na2Cr2O7 | |||
| 550 à 580 kg | 15 à 30 kg | 15 à 30 kg | 0,01 à 0,15 kg |
L’électricité représente de 70 à 85 % des coût de production, le sel, 10 %.
Souvent, la production de chlorate de sodium est effectuée sur les lieux d’élaboration de la pâte à papier, principaux consommateurs de ce produit.
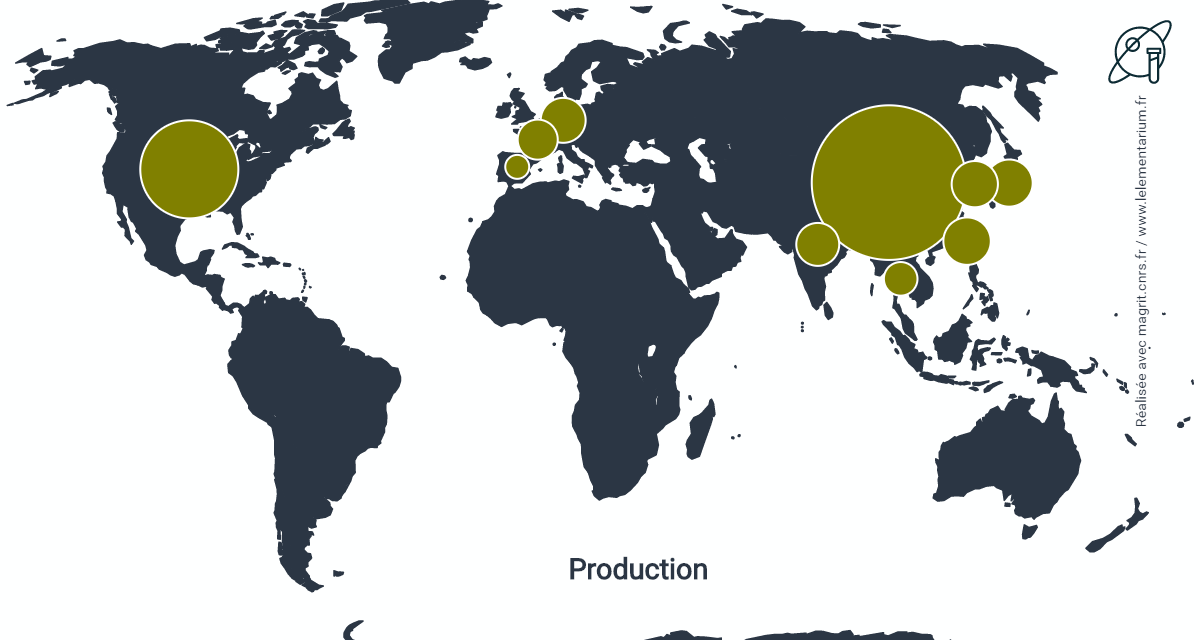
Productions
Les capacités mondiales de production sont estimées, en 2013, à environ 4 millions de t/an avec :
| Canada | 1 200 000 | Chine | 280 000 | |
| États-Unis | 830 000 | Russie | 100 000 | |
| Europe | 710 000 | Japon | 33 000 | |
| Amérique du sud | 450 000 | Autres pays asiatiques | 145 000 |
En 2017, la production mondiale a été de 3,6 millions de t.
Dans l’Union européenne, en 2019, la production (qui regroupe celles de chlorates, perchlorates, bromates, perbromates, iodates et periodates) est de 799 682 t dont :
| Finlande | 316 639 | Suède (estimation) | 100 000 | |
| France | 122 682 | Espagne | 38 971 |
Commerce international : en 2019.
Principaux pays exportateurs : sur un total de 626 420 t.
| Canada | 507 159 | Brésil | 14 500 | |
| États-Unis | 47 997 | Chine | 12 322 | |
| Espagne | 15 226 | Ouzbékistan | 7 878 |
Source : ITC
Les exportations du Canada sont destinées aux États-Unis à 84 %, au Japon à 9 %.
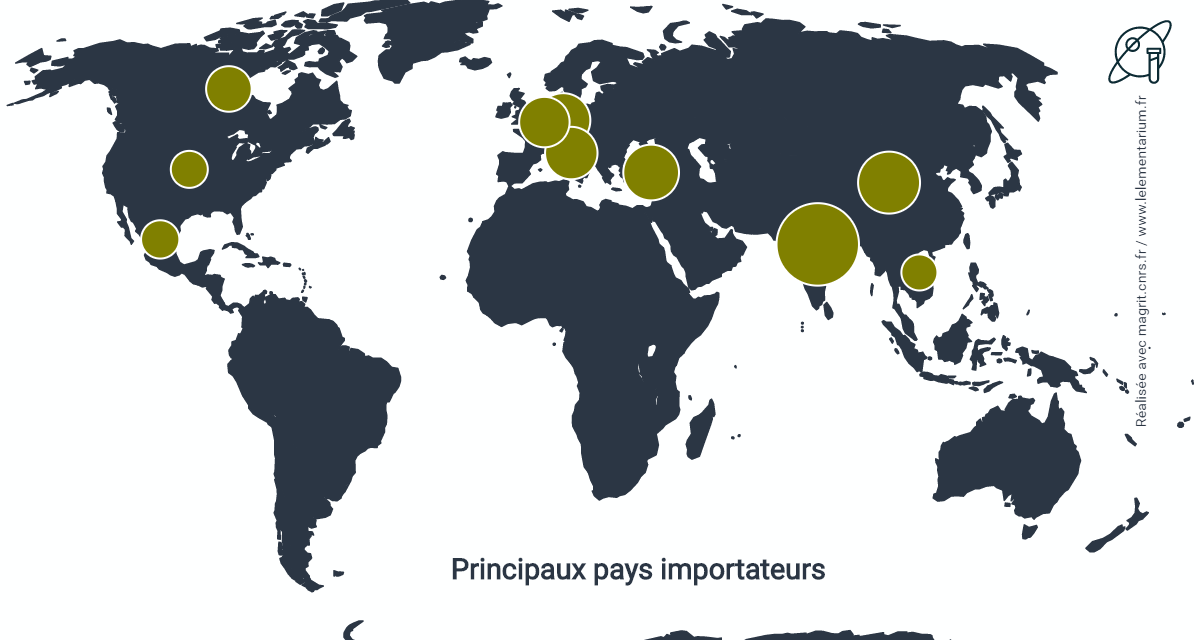
Principaux pays importateurs :
| États-Unis | 471 668 | Portugal | 33 235 | |
| Japon | 74 334 | Inde | 23 194 | |
| Russie | 38 855 | Thaïlande | 20 723 |
Source : ITC
Les importations des États-Unis proviennent du Canada à 99,7 %.
Principaux producteurs :
- Eka, filiale du groupe néerlandais Nouryon, n°1 mondial avec 24 % du marché, possède une capacité de production de 900 000 t/an, avec aux États-Unis, 200 000 t/an à Columbus dans l’État du Mississippi et 63 000 t/an à Moses Lake dans l’État de Washington, au Canada, dans la province de Québec, 118 000 t/an à Valleyfield et 150 000 t/an à Magog, en France, 70 000 t/an à Ambès (33), en Suède, 72 000 t/an à Alby et Stockvik, en Finlande, à Oulu, au Brésil, à Jundiai et Bahia, au Chili, à Talcahuano, en Russie, à Koryazhma dans la région d’Arkhangelsk.
- Erco Worldwide, division du groupe canadien Superior Plus, n°2 mondial avec 17 % du marché, possède 515 000 t/an de capacité de production et a vendu, en 2019, 480 000 t, avec des usines au Canada, à Buckingham (130 000 t/an), au Québec, Hargrave (40 000 t/an), au Manitoba, Vancouver (100 000 t/an), en Colombie Britannique, Grande Prairie (50 000 t/an), en Alberta, Thunder Bay, dans l’Ontario, aux États-Unis, à Valdosta (100 000 t/an), en Georgie et au Chili, à Mininco (55 000 t/an).
- Kemira, n°3 mondial avec 15 % du marché, possède des unités de production en Finlande (235 000 t/an), à Joutseno et Sastamala, aux États-Unis, à Augusta (132 000 t/an) en Georgie et Eastover (82 000 t/an) en Caroline du Sud, en Uruguay, à Fray Bentos et au Brésil, à Ortigueira, dans l’État de Paraná.
- Chemtrade, société canadienne, qui exploitait une unité de production au Canada, à Prince George, en Colombie Britannique, avec 78 000 t/an, a acquis, en mars 2017, la société Canexus, n°4 mondial, avec 11 % du marché, avec des usines au Canada, à Brandon (320 000 t/an) dans le Manitoba, Beauharnois (44 000 t/an) au Québec et au Brésil, à Espírito Santo (66 000 t/an). L’usine de Bradon, est la plus importante, dans le monde. En 2019, les ventes nord-américaines ont été de 392 000 t.
- Autres producteurs : China First Chemical Holdings (Chine), Arkema (France) avec 85 000 t/an, Ercros (Espagne), à Sabiñánigo, province de Huesca, avec 46 000 t/an.
Situation française
En 2019.
Production : 122 682 t de chlorates, perchlorates, bromates, perbromates, iodates et periodates.
Producteurs :
- Arkema avec une capacité de production de 85 000 t/an à Jarrie (38).
- Eka, filiale de Nouryon, avec une capacité de production de 70 000 t/an à Ambès (33).
Commerce extérieur :
Les exportations sont confidentielles.
Les importations s’élevaient à 7 120 t en provenance principalement à :
- 90 % d’Espagne,
- 6 % de Finlande.
Utilisations
Consommations
Dans le monde, en 2019 : 4,2 millions de t, dont 1,4 million de t en Amérique du Nord.
Secteurs d’utilisation
Dans le monde, en 2018, plus de 90 % de la production est destinée au blanchiment de la pâte à papier.
Industrie de la pâte à papier : NaClO3 donne in situ, en milieu acide, du dioxyde de chlore (ClO2, gaz explosif ne pouvant être ni stocké ni transporté) utilisé dans le blanchiment des pâtes chimiques (pâtes kraft et pâtes au bisulfite). On obtient ainsi les pâtes ECF (Elemental Chlorine Free).
ClO3– + 2 HCl = ClO2 + 1/2 Cl2 + Cl– + H2O
La consommation moyenne de NaClO3 est de 20 kg par tonne de pâte, il représente 5 % du coût de fabrication de la pâte à papier.
La production mondiale de pâtes chimiques a été, en 2010, de 130 millions de t (142 millions de t en 2017) dont 95,5 millions de t (102 millions de t en 2017) ont été blanchies avec 88,3 millions de t pour les pâtes ECF (Elemental Chlorine Free), 4,8 millions de t pour les pâtes TCF (Totally Chlorine Free) traitées par l’ozone ou l’eau oxygénée et 2,4 millions de t pour les pâtes utilisant le dichlore. L’utilisation du dichlore a été fortement réduite afin d’éviter la formation de composés organochlorés et en particulier de dioxines.
Évolution mondiale de la production de la pâte à papier chimique en fonction du mode de blanchiment :
| 1990 | 2000 | 2005 | 2010 | 2012 | |
| Total | 68,6 | 83,1 | 91,5 | 95,5 | 101,0 |
| Dichlore | 64,0 | 21,2 | 10,0 | 2,4 | 2,4 |
| ECF | 4,4 | 53,9 | 75,6 | 88,3 | 93,9 |
| TCF | 0,2 | 6,0 | 5,9 | 4,8 | 4,7 |
Production de pâte à papier, en 2012, en Amérique du Nord et en Scandinavie en fonction du mode de blanchiment :
| Amérique du Nord | Scandinavie | ||
| Total | 33,9 | 12,8 | |
| Dichlore | 0,4 | 0,0 | |
| ECF | 33,4 | 10,0 | |
| TCF | 0,1 | 2,8 |
Élaboration de dérivés chimiques :
- Chlorate de potassium (KClO3) destiné principalement à la fabrication des allumettes, voir ce produit.
- Perchlorate de sodium (NaClO4) : obtenu par oxydation électrolytique d’une solution de NaClO3. En France, production par Arkema à Jarrie (38) avec une capacité de 8 000 t/an. Aux États-Unis, la production est assurée par American Pacific, à Cedar City dans l’Utah. Il est utilisé dans la fabrication de bouillies explosives et comme intermédiaire dans la fabrication du perchlorate d’ammonium.
- Perchlorate d’ammonium (NH4ClO4) : il est obtenu à partir du perchlorate de sodium, en présence de chlorure d’ammonium, par double décomposition, selon la réaction suivante :
NaClO4 + NH4Cl = NH4ClO4 + NaCl
Safran Ceramics, société du groupe Safran, n°2 mondial, est le seul producteur européen avec une capacité de 4 000 t/an à Saint Médard en Jalles (33). Le n°1 mondial est American Pacific, seule société productrice aux États-Unis, à Iron County dans l’Utah, avec 13 600 t/an de capacité de production.
La consommation française est d’environ 3 000 t/an en particulier pour les « boosters » d’Ariane 5, les missiles M45 des sous-marins nucléaires lanceurs d’engins et les systèmes de déclenchement des « airbags ».
Le perchlorate d’ammonium (NH4ClO4) entre à 68 % dans les 237 t de propergol solide (poudre), en présence de polybutadiène (14 %) et de poudre d’aluminium (18 %), utilisées dans les « boosters » d’Ariane 5. La combustion doit durer 123 s et assurer 92 % de la poussée du lanceur au décollage. Chaque seconde, expulsion de 1,9 t de gaz à 3000 K provenant, en partie, de la réaction suivante :
6 NH4ClO4 + 10 Al = 3 N2 + 9 H2O + 5 Al2O3 + 6 HCl
- Perchlorate de potassium (KClO4), utilisé en pyrotechnie civile dans les feux d’artifice. La production du groupe chinois HHH est de 10 000 t/an.
- Chlorite de sodium (NaClO2) : il est obtenu par réduction à l’aide de SO2, HCl, H2O2 ou de méthanol, de solutions de NaClO3. Le procédé Arkema utilise une réduction par H2O2, en deux étapes. Dans un premier temps, en présence d’acide sulfurique et d’air pour diluer ClO2 et ainsi éviter les risques d’explosion, du dioxyde de chlore est formé :
2 ClO3– + H2O2 + 2 H3O+ = 2ClO2 + 4 H2O + O2
Ensuite, les gaz sont lavés puis ClO2 est réduit dans des colonnes d’absorption en présence de soude :
2 ClO2 + H2O2 + 2 OH– = 2 ClO2– + O2 + 2 H2O
En général, le chlorite de sodium est obtenu et commercialisé en solution concentrée.
En Amérique du Nord, en 2017, la demande est de 15 000 à 20 000 t/an. Erco Worldwide, division du groupe canadien Superior Plus, possède une capacité de production de 10 000 t/an, au Canada, à Buckingham, au Québec et Thunder Bay, dans l’Ontario et a vendu, en 2017, 7 600 t. A acquis, en octobre 2017, auprès du groupe Lanxess, la société International Dioxide qui possède une unité de production, aux États-Unis, à North Kingstown dans le Rhode Island.
Le chlorite de sodium est principalement utilisé pour former, in situ, du dioxyde de chlore employé pour la purification de l’eau, dans des installations de faible capacité, ou le blanchiment des textiles. La média-mutation de ClO2– en ClO2 est réalisée par HCl ou Cl2.
5 ClO2– + 4 H3O+ = 4 ClO2 + Cl– + 6 H2O
Il est utilisé également dans la synthèse de colorants, les traitements de surfaces…
Minerai d’uranium : NaClO3 est utilisé dans le traitement acide du minerai (1 à 2 kg/t de minerai). Dans cette application il est concurrencé par d’autres oxydants : pyrolusite (MnO2), HNO3 (voir le chapitre consacré à l’uranium).
Pyrotechnie : utilisé principalement en Chine directement dans les feux d’artifice ou après transformation en chlorate de potassium.
Le rôle des ions ClO3– dans le désherbage est lié à leur structure, analogue à celle des ions NO3– utilisés comme engrais. Ces derniers sont assimilés par les racines des plantes puis réduits en ions nitrite (NO2–), cette réduction étant catalysée par une enzyme, la nitrate réductase. Dans le cas des ions chlorates, la réduction par la nitrate réductase donne des ions chlorite (ClO2–) ce qui a pour effet de tuer les cellules dans lesquelles s’effectue cette réaction.
Générateur chimique de dioxygène : dans les avions, face aux risques de dépressurisation, du dioxygène peut être fourni par des générateurs destinés à alimenter 2,3 ou 4 passagers, avec 21 L/personne pendant au moins 15 minutes. Le générateur se déclenche automatiquement à l’aide d’un capteur de pression. Il renferme un mélange de chlorate de sodium et d’environ 8 % de poudre de fer qui, à 260°C, libère du dioxygène. Le dioxygène provient de la décomposition thermique du chlorate de sodium selon la réaction :
NaClO3 = 3/2 O2 + NaCl
La poudre de fer catalyse la réaction. De 2 à 6 % de dioxyde de baryum est ajouté afin de fixer le dichlore qui peut se former.
Bibliographie
- Syndicat des Halogènes et Dérivés (SHD), Immeuble diamant A, 14, rue de la République, 92909 Paris la Défense Cedex.
- Euro Chlor, Avenue E Van Nieuwenhuyse 4, box 2, B-1160 Brussels, Belgique.
- Alliance for Environmental Technology.
- Product information manual, sodium chlorate, Nouryon.
- Reference Document on Best Available Techniques for the Manufacture of Large Volume Inorganic Chemicals – Solids and Others Industry, UE, Octobre 2006.
- Best Available Techniques (BAT) Reference document for the production of pulp, paper and board, Commission européenne, 2015.
- INERIS, 2012. Données technico-économiques sur les substances chimiques en France : Perchlorate d’ammonium, DRC-12-126866-07629A, 67 p.
- Désinfection de l’eau par le dioxyde de chlore, Lenntech, Rotterdamseweg 402 M, 2629 HH Deft, Pays-Bas.


Commentaires récents